| chimica |
|
PRINCIPI DI CHIMICA GENERALE
Elementi: costituiscono la materia ed in natura ne troviamo una novantina (Carbonio, Ossigeno, Calcio, Ferro, . ).
Atomo: è l'unità costituente della materia, l'unità che forma gli elementi chimici e la più piccola particella di elemento che possiede le proprietà di tale elemento. Ogni atomo possiede un nucleo dove si collocano particelle cariche positivamente e particelle ellettricamente neutre : protoni (+) con compito di attirare elettroni permettendo all'atomo di identificarsi e neutroni (0) con il compito di evitare forze repulsive tra protoni. Intorno all'atomo orbitano leggerissime particelle di massa trascurabile cariche negativamente: elettroni (-). Il numero di protoni ed elettroni in 1 atomo è lo stesso e risulta quindi elettricamente neutro. Un atomo con il medesimo n° di protoni dell'elemento a cui appartiene ma con numero di neutroni diverso si definisce isotopo. Tutti gli atomi di un dato elemento hanno stesso numero atomico (Z: n° protoni e elettroni). Isotopi di uno stesso elemento differiscono per numero di massa (somma protoni e neutroni). Esiste anche il peso atomico (valore relativo ottenuto prendendo come riferimento la massa del carbonio-l2). Molti isotopi sono radioattivi poiché il nucleo è instabile ed emette energia nel passare a forma più stabile. Gli atomi sono costituiti principalmente da spazio vuoto. Gli elettroni si muovono ad una velocità pari a quella della luce. È difficile sapere dove si trova in ogni istante, x questo si parla di nuvola elettronica. La distanza media di un elettrone da nucleo dipende da sua energia: maggiore è energia, maggiore è distanza dal nucleo. Elettrone con bassa energia si trova vicino a nucleo, elettrone con alta energia si trova ad un livello d'energia + alto. Un elettrone x passare ad un livello energetico più alto deve assorbire energia, x passare a livello + basso deve rilasciare parte dell'energia posseduta. Elettrone che occupa livello + basso si trova nel suo stato fondamentale ed assorbe energia radiante fino a quando passa a livello + alto in uno stato eccitato dove cede energia assorbita all'ambiente. Quando tutti gli elettroni si trovano nei livelli di energia + bassa l'atomo ha la massima stabilità. Ogni livello energetico ha 1 limite di contenimento di elettroni (1°: max. 2; 2° e 3°: max. 8) e tutti i livelli energetici sono rappresentati mediante circonferenze concentriche al nucleo sulle quali si dispongono gli elettroni.
1870: chimico russo Dmitrij Mendeleev costruì tabella che tenesse conto delle analogie nei comportamenti chimici dei vari elementi.
Questa tavola prese il nome di TAVOLA PERIODICA DEGLI ELEMENTI e gli elementi sono ordinati secondo il loro numero atomico crescente e riportati con il proprio simbolo, nome, peso atomico e indicazioni sul loro livello d'energia + esterno. Su ciascuna riga (periodo) ci sono elementi che riempiono lo stesso livello energetico
(1°,2°,3°, . ). Idrogeno e Elio (1° livello), dal Litio al Neon (2° livello), . . Su ciascuna colonna (gruppo) ci sono elementi che possiedono atomi con stesso numero di elettroni nel livello energetico + esterno e quindi con stesso comportamento chimico. Fluoro, Cloro e Bromo (alogeni), hanno tutti 7 elettroni nel livello + esterno: basta uno in + x far diventare l'atomo stabile. Atomo stabile è difficile che reagisca.
Atomi con livello energetico esterno riempito solo parzialmente tendono a reagire con altri atomi x completare proprio livello più esterno. Alcuni quindi cedono elettroni, altri tendono ad acquistarli e altri ancora tendono a mettere in comune i propri elettroni.
Molecole: particelle formate da 2 o + atomi collegati da legami covalenti (che mettono in comune degli elettroni)
Composto chimico sostanza che contiene atomi di 2 o + elementi chimici differenti, tenuti uniti da legami chimici in proporzione definitiva e costante.
1911: Modello elettronico di Rutherford: propose il modello nucleare dell'atomo ipotizzando che l'atomo sia una sorta di sistema etario in miniatura dove elettroni orbitano attorno al nucleo lungo traiettorie note e prevedibili e orbite ellittiche (ma ciò non è vero poiché nucleo perderebbe energia e si collasserebbe)
1913: Modello elettronico di Bohr: secondo lui l'energia è quantizzata (x 1 elettone in 1 atomo non sono disponibili tutti i possibili valori di energia, ma solo alcuni). Gli elettroni degli atomi non viaggiano su un orbita costante e fissa ma l'elettrone occupa un orbitale (spazio dove elettrone può trovarsi con una probabilità del 90%) [meccanica quantistica]. Nelle molecole gli orbitali di un dato atomo si mescolano fra loro e formano orbitali ibridi.
LEGAMI:
- LEGAME IONICO: legame abbastanza forte che comporta reciproca attrazione tra IONI (atomi che hanno acquistato o ceduto elettroni;
particelle con cariche elettricamente + o -) di carica opposta: ione + (catione): possiede + protoni e - neutroni; ione - (anione): possiede - protoni e + neutroni .
- LEGAME COVALENTE: legame chimico molto forte e stabile formato da coppie condivise di elettroni. Si divide in:
POLARE: quando si legano 2 atomi con diversa elettronegatività (con atomi di diversi elementi) e formano una molecola con propria polarità interna e presenta regioni
con parziale carica positiva e regioni con parziale carica negativa. Es: molecola triatomica dell'acqua: legame O - H è polare.
APOLARE: quando si legano 2 atomi con stessa elettronegatività (atomi di stesso tipo) condividendo elettroni dell'ultimo livello. Non c'è polarità. Nuclei degli atomi
attirano on stessa forza gli elettroni di legame e la nube elettronica (luogo dove orbitano elettroni x formare l'ottetto e un orbitale molecolare) è asimmetrica. Non c'è distribuzione di carica a una delle loro estremità. Sono non polari tutte le molecole biatomiche formate da due atomi dello stesso tipo. Es: molecola triatomica dell'anidride carbonica è apolare x sua geometria lineare.
- SEMPLICE: 3 atomi completano loro livelli energetici + esterni e c'è condivisione di 1 coppia di elettroni (1 atomo: 1elettrone)
- DOPPIO: c'è condivisione di 2 coppie di elettroni.
- TRIPLO: c'è condivisione di 3 coppie di elettroni.
REAZIONI CHIMICHE: sono sistemi x trasformare la materia e sono rappresentate mediante equazioni chimiche bilanciate (xchè il numero e tipo di atomi dei prodotti deve corrispondere a quello iniziale dei reagenti). Per indicare la direzione della trasformazione chimica si utilizza la freccia. 1 freccia: irreversibilità; 2 frecce: reversibilità. A sinistra della freccia si trovano i reagenti (A+B) mentre a destra i prodotti (C+D). Per permettere alla reazione di essere bilanciata bisogna aggiungere coefficienti stechiometrici. La materia trasformata infatti non è sempre bilanciata a causa di scambi energetici.
ELEMENTI BIOLOGICAMENTE IMPORTANTI: Carbonio (C), Idrogeno (H), Azoto (N), Ossigeno (O), Fosforo (P), Zolfo (S): formano insieme l'acronimo CHNOPS e sono usati x costruire macromolecole biologiche. Non sono stabili e spesso formano legami covalenti forti e stabili a causa degli elettroni molto vicini al nucleo e atomi piccoli e leggeri. Tutti gli elementi tranne l'idrogeno possono formare legami con 2 o + atomi formando molecole complesse necessarie x la struttura e le funzioni dei sistemi viventi.
STRUTTURA MOLECOLARE DELL'ACQUA:
E' costituita da 2 atomi di idrogeno e 1 di ossigeno legati da 1 legame covalente. E' una molecola neutra (con uguale numero di elettroni e protoni), polare e con 4 vertici: 2 di carica + e 2 di carica -. Quando un vertice negativo di una molecola d'acqua si avvicina ad un vertice positivo di un'altra molecola d'acqua attraendosi, si forma un LEGAME IDROGENO (legame di natura elettrostatica). Tutte le molecole d'acqua sono aggregate fra loro in natura e ognuna di esse si lega con almeno altre 4. L'idrogeno fa da parete tra le 2 molecole. Il legame idrogeno è molto + debole del legame ionico e covalente ed è di breve durata (1 centomiliardesimo di secondo) ma una volta spezzato tende subito a riformarsi tra molecole diverse. I legami idrogeno variano al variare della temperatura e della pressione e rendono possibili gli effetti di forze di coesione.
LE PROPRIETA' DELL'ACQUA:
sono: tensione superficiale, capillarità e imbibizione, elevato calore specifico, elevato calore di evaporazione e solidificazione e ottimo solvente.
1) TENSIONE SUPERFICIALE: è una conseguenza dell'attrazione reciproca delle molecole d'acqua determinata dall'instaurarsi dei legami idrogeno. Tale attrazione se si verifica tra molecole della stessa sostanza è detta coesione, se si verifica con altre molecole polari e superfici dotate di carica è detta adesione.
2) CAPILLARITA' : capacità che ha l'acqua di muoversi all'interno di spazi piccolissimi (tubicini) vincendo la forza gravitazionale. IMBIBIZIONE: consiste nel movimento capillare delle molecole d'acqua dentro sostanze (legno, gelatina) che aumentano di volume. La pressione può essere molto elevata.
3) ELEVATO CALORE SPECIFICO (capacità termica): l'acqua è il liquido a + elevato calore specifico (ad eccezione della ammoniaca). Per alzare o abbassare di 1 grado un grammo di H20 bisogna aggiungere / sottrarre ben 1 caloria (quantità di calore). Il calore specifico dell'acqua è 4 volte quello dell'aria, 10 volte quello del ferro, doppio dell'alcool o dell'olio (occorre solo mezza cal). Le molecole dell'acqua sono in continuo movimento influenzato dalla temperatura: trasferendo calore aumenta l'energia cinetica ovvero aumentano i movimenti delle molecole, al diminuire le particelle rallentano. Energia termica: forma di energia che ogni corpo possiede e che è dovuta all'incessante movimento di tutte le particelle che lo costituiscono. Tale energia è infatti associata alla temperatura dei corpi. All'aumentare della temperatura aumenta l'energia termica. Temperatura: numero che esprime il valore dell'energia cinetica media delle particelle che costituiscono un corpo. L'energia termica è la somma dell'energia cinetica di tutte le particelle.
L'elevato calore specifico dell'acqua è dovuto ai legami idrogeno fra le molecole poiché essi tendono a limitare il numero delle molecole. Per aumentare di 1 grado la temperatura dell'acqua bisogna infatti rompere i legami idrogeno delle molecole. Gran parte del calore fornito è impiegato x rompere i legami, piccola parte x accelerare movimenti molecole.
4) ELEVATO CALORE DI EVAPORAZIONE: è il passaggio dallo stato liquido a quello gassoso di una sostanza dovuto a energia. 1 grammo di acqua x evaporare (a 100° C) con una pressione di 1 atmosfera, occorrono 540 calorie. Avviene quando alcune molecole si staccano dalla superficie del liquido e passano nell'aria. + alta è temperatura del liquido e + rapidi sono i movimenti delle particelle e la velocità di evaporazione. Anche qui l'elevato calore di evaporazione è dovuto ai legami idrogeno che devono essere spezzati. L'evaporazione è anche un modo con cui gli organismi stabilizzano la propria temperatura corporea.
5) SOLIDIFICAZIONE (congelamento): è il passaggio dallo stato liquido a quello solido di una sostanza conseguente alla riduzione dell'energia cinetica. Al di sotto dei 4° C iniziano a distanziarsi l'una dall'altra x cercare di mantenere il maggior numero possibile di legami idrogeno all'interno di una struttura stabile. A 0° C (punto di solidificazione dell'acqua) si forma un solido cristallino dove ogni molecola è legata con legami idrogeno permanenti con altre 4 molecole d'acqua molto + distanti fra loro rispetto allo stato liquido. Il ghiaccio è meno denso ma occupa + volume dell'acqua liquida. Passando nuovamente allo stato liquido, rompendo i legami idrogeni del reticolo cristallino, sottrae calore dall'ambiente circostante. Mentre nel passare allo stato solido libera energia calore nell'ambiente circostante. Grazie all'elevato calore di solidificazione i cambiamenti di temperatura sono + frenati e organismi possono adattarsi al cambiamento delle stagioni.
6) OTTIMO SOLVENTE:
SOLVENTE: sostanza presente in maggiore quantità; SOLUTO: sostanza presente in minore quantità; SOLUZIONE: miscuglio omogeneo di 2 o + sostanze. SOLUBILITA': quantità in grammi di soluto che riesce a sciogliersi in 100 g di solvente ad una determinata temperatura e pressione x soluti gassosi.
L'acqua è un ottimo solvente grazie alla polarità delle sue molecole. Essa si lega con sostanze idrofile (che possono legarsi con l'acqua e formare soluzioni); es: zucchero o sale da cucina: loro cristalli si disgregano e ogni molecola sciolta viene circondata da molecole di acqua con cui potrà legarsi formando legami idrogeno temporanei. Non si lega con sostanze non polari o idrofobe (non formano soluzioni acquose).
IONIZZAZIONE DELL'ACQUA:
Ad una certa temperatura allo stato liquido, alcune molecole tendono a ionizzarsi: un atomo di idrogeno ha una debole tendenza a lasciare l'atomo di ossigeno, al quale è collegato x mezzo del legame covalente e a passare in soluzione sotto forma di ione H+: molto reattivo e si lega con legame covalente dativo all'ossigeno di un'altra molecola formando 2 ioni complessi detti idronio (H3O) e ossidrile (OH-). Tale tendenza a ionizzarsi è bilanciata dalla tendenza degli ioni a riassociarsi fra loro [situazione di equilibrio dinamico: avvengon 2 processi l'uno l'opposto dell'altro]. Nell'acqua pura in condizioni di equilibrio solo una piccola parte è nella forma ionizzata, mentre la maggior parte è nella forma molecolare.
ACIDI E BASI:
ACIDO: sostanza che provoca aumento della concentrazione relativa di ioni H+ in una soluzione. Sostanza acida: concentrazione ioni H+ supera quella degli ioni OH-
BASE: sostanza che provoca aumento della concentrazione relativa di ioni OH- in una soluzione. Sostanza basica: concentrazione ioni OH- supera quella degli ioni H+.
Messa in acqua libera ioni OH-. Es: idrossido di sodio (molecola polare basica idrofila: NaOHà si dissocia in Na+ e OH-).
Esistono acidi e basi forti: sostanze come acido cloridrico che si ionizzano quasi completamente in acqua, facendo aumentare in modo considerevole la concentrazione, rispettivamente, degli ioni H+ e OH-. Esistono anche acidi e basi deboli: sostanze che si ionizzano solo parzialmente, facendo così aumentare debolmente la concentrazione degli ioni H+ e OH-.
Per esprimere il grado di acidità delle sostanze si utilizza la scala del pH (unità di misura x stabilire grado di acidità o basicità di una soluzione con concentrazione di ioni H+) che normalmente varia da 0 (acidi forti) a 14 (basi forti). A pH 7 [condizione di neutralità] ioni H+ e OH- hanno la stessa concentrazione (es: acqua pura: ioni H+ = ioni OH-). Ogni pH inferiore a 7 è acido e ogni pH superiore a 7 è basico. 1 unità di pH corrisponde a 10 volte la concentrazione di ioni H+. La maggior parte delle reazioni chimiche ha luogo all'interno di un ristretto intervallo di pH prossimo alla neutralità.
MACROMOLECOLE BIOLOGICHE:
Sono molecole organiche contenenti carbonio.
CARBONIO: si lega all'idrogeno (in legami semplici), ossigeno, azoto, fosforo, zolfo x formare macromolecole organiche ed è tra gli elementi + presenti sulla terra. Può formare fino a 4 legami e mediante legami semplici, doppi (no carbonio-idrogeno) e tripli (legame + forte in assoluto: specificità del carbonio).
Organismo vivente: costituito da acqua (50-95%), sodio, potassio, calcio (1%) e molecole organiche (parte restante).
SCHELETRO CARBONIOSO: struttura portante della macromolecola biologica composta da atomi di carbonio al quale si posson legare altri composti costituiti da atomi di azoto e ossigeno che formano gruppi funzionali. Esso determina molte proprietà e funzioni all'interno dei sistemi viventi. Le molecole in organismi viventi possono essere rappresentate sottoforma di formule grezze (specificano numero di atomi di ogni elemento chimico presente nella molecola: Cn(H2O)) o mediante formule di struttura (evidenziano in che modo tali atomi sono collegati fra loro: per rappresentare un legame covalente semplice si rappresenta un tratto singolo, x legame covalente doppio si rappresenta un tratto doppio; es: H - C - H).
ISOMERI: sostanze costituite da molecole con stessa formula grezza ma diversa formula di struttura. Es: glucosio e fruttosio (hanno stessa formula grezza, ma atomi di carbonio che formano il doppio legame con l'ossigeno sono in posizione differente e quindi presentano diversa formula di struttura). Glucosio e fruttosio, messe in acqua tendono a ripiegarsi formando strutture chiuse ad anello [FORMULA CICLICA: rappresentazione di 1 poligono con tanti vertici quanti sono atomi di C nell'anello].
FORMULE CHIMICHE E GRUPPI FUNZIONALI:
- Molecole organiche + semplici: IDROCARBURI: composti costituiti solo da carbonio e idrogeno usati x produrre energia (es: metano). Essi derivano da resti di organismi morti milioni di anni fa che, in particolari condizioni ambientali, hanno svolto un lungo processo di fossilizzazione che li ha trasformati in carbonio e petrolio.
- Molecole organiche + complesse: caratterizzate da particolari gruppi di atomi legati allo scheletro carbonioso: GRUPPI FUNZIONALI:
Il gruppo ossidrilico: formato da 1 atomo di ossigeno e 1 di idrogeno, è polare e caratterizza gli alcoli (es: alcool etilico).
Il gruppo carbonilico: caratterizzato da un atomo di ossigeno legato al carbonio da un doppio legame covalente, è presente nelle aldeidi (gruppo: è all'estremità dello
scheletro carbonioso; es: glucosio) o nei chetoni (gruppo: è su un atomo di carbonio interno alla catena; es: fruttosio).
Il gruppo carbossilico: formato da un gruppo carbonilico cui è legato un gruppo ossidrilico, caratterizza gli acidi organici o acidi carbossilici.
Il gruppo amminico: formato da un atomo di azoto su cui si possono legare fino a 2 atomi di idrogeno, rende la molecola basica (attrae ioni idrogeno) e suoi composti
organici si chiamano ammine.
Le molecole organiche spesso sono grosse e complesse in quanto sono costituite da migliaia di atomi e costituite da polimeri (unione di + monomeri).
CARBOIDRATI (zuccheri):
Principali molecole di riserva energetica della maggior parte degli esseri viventi. Principali funzioni:
1) principale fonte energetica (molecole: usate quando organismo ha bisogno di energia).
2) utili a realizzare strutture cellulari (es. chitina, cellulosa, . ).
3) utili a realizzare altre molecole biologiche (es. ribosio e desossiribosio: usati x costruire acidi nucleici).
Esistono 3 tipi di carboidrati classificati secondo il numero di molecole che contengono:
- MONOSACCARIDI [zuccheri semplici costituiti da 1 sola molecola e rappresentano i monomeri degli zuccheri + complessi; es: ribosio, desossiribosio, galattosio, glucosio (principale fonte di energia x maggior parte cellula - STRUTTURA DELLE CELLULE EUCARIOTE" class="text">delle cellule e nei vertebrati è il normale zucchero di trasporto portato dal sangue e raggiungendo tutte le cellule x rifornirle di energia), fruttosio (presente nella frutta)].
- DISACCARIDI (formati da 2 monosaccaridi uniti da 1 legame covalente; es: saccarosio e lattosio).
- POLISACCARIDI (contengono polimeri: molti monosaccaridi legati tra loro; es: cellulosa e amido).
MONOSACCARIDI:
- composti organici formati da carbonio, idrogeno e ossigeno. Un atomo di carbonio si lega con 2 di idrogeno e 1 di ossigeno.
- sono il materiale da costruzione con cui le cellule fabbricano i polisaccaridi e altre molecole essenziali e principale fonte di energia x la maggior parte degli organismi.
- in essi può succedere che legami fra atomi si spezzino a causa dell'energia cinetica da loro prodotta. Le forze di legame vengono misurate in kilocalorie x mole (quantità di sostanza che contiene un numero costante di molecole) che rappresentano la quantità di energia che deve essere somministrata x spezzare il legame in condizioni di ambiente e pressione standard. + è forte il legame, maggiore energia deve essere impiegata x romperlo; i legami covalenti doppi sono + forti di quelli semplici e legame semplice tra carbonio e idrogeno è + forte rispetto carbonio-ossigeno e carbonio-carbonio.
Quando legame covalente si spezza: atomi si separano e ciascuno si riprende proprio elettrone e atomi tornano a riavere livelli energetici esterni incompleti sin a quando non riformeranno nuovi legami covalenti e ripristinando conurazione stabile con livelli energetici esterni ancora completi. A stabilire se nuovo legame è identico a precedente sono fattori come temperatura, pressione e tipo di atomo a disposizione nelle vicinanze. Se nuovo legame è diverso e è debole di quello precedente la reazione libera energia nell'ambiente mentre se è + forte viene sottratta energia dall'ambiente.
Es: 1) Fotosintesi clorofilliana: si prende energia radiante x rompere e ricostruire legami covalenti (acqua + anidride carbonica + energiaà glucosio + ossigeno).
2) Respirazione cellulare: si libera energia nell'ambiente x rompere e ricostruire legami covalenti (glucosio + ossigenoà acqua + anidride carbonica + energia)
- anche altre sostanze organiche (legno, benzina, alcool, . ) liberano energia immagazzinata nelle loro molecole quando vengon demolite.
- Glucosio: zucchero presente nella frutta e prodotto dalla fotosintesi. Viene demolito nella respirazione cellulare x ricavare energia (40% di essa viene
immagazzinata nuovamente nei legami di altre molecole organiche). Nell'uomo è normale zucchero di trasporto che raggiunge e rifornisce di energia
tutte le cellule grazie al sangue.
- Fruttosio: è un isomero del glucosio; presente nella frutta: è sostanza che rende dolce il miele.
DISACCARIDI:
- composti organici formati da 2 molecole di monosaccaridi legati da un legame covalente.
Es: Saccarosio: zucchero da tavola formato dalla condensazione (unione) di 1 molecola di glucosio e 1 di fruttosio, presente nella linfa delle piante, trasportato dalle cellule fotosintetiche e usato come fonte energetica. Per permettere il legame covalente fra fruttosio e glucosio deve avvenire una reazione di condensazione (2 monosaccaridi eliminano 1 molecola d'acqua; atomo di ossigeno fa da ponte tra 2 molecole di zucchero formando un nuovo legame: legame glicosilico covalente: reazione chimica che determina la sintesi di molti polimeri organici a partire dalle loro unità base; usato x costruire legami complessi). Se disaccaride che si forma è scisso nei monosaccaridi che lo costituiscono viene aggiunta 1 molecola d'acqua e tale scissione dell'acqua è detta idrolisi (reazione che prevede l'aggiunta di acqua x scindere legami glicosilici e liberare quindi energia).
Trealosio zucchero trasportato nel sangue insetti costituito da legame di 2 molecole di glucosio); Lattosio: zucchero che si trova solo nel latte costituito da 1 molecola di glucosio legata ad 1 di galattosio. Non x tutti è digeribile.
POLISACCARIDI:
- composti organici formati da molte unità (molecole) di monosaccaridi uguali e diversi (possono essere anche centinaia o migliaia) legati in lunghe catene.
Es: Amido (principale polisaccaride di riserva delle piante, realizzato legando centinaia di unità di glucosio e presente nelle cellule fotosintetiche sottoforma di piccoli granuli (consistenza granulosa: molecole di glucosio assumono forma tridimensionale). E' presente negli amminoplasti.
Glicogeno: principale zucchero di riserva degli animali e dei funghi. Differisce dall'amido nella lunghezza delle catene polisaccaridiche e nel modo in cui le molecole di glucosio sono legate fra loro. X essere usati come fonte energetica devono essere idrolizzati in monosaccaridi o disaccaridi.
Cellulosa zucchero di struttura presente nei vegetali. È il costituente principale delle pareti delle cellule vegetali ed è 1 polimero del glucosio. I legami che uniscono unità di glucosio sono differenti da quelli dell'amido e del glicogeno: tale differenza rende diversa anche la struttura tridimensionale e le proprietà delle molecole: il glucosio ha un aspetto fibroso (molecole: formano cioè lunghi fasci rigidi che rendon struttura molto resistente). È difficilmente idrolizzabile (solo pochi microrganismi posson idrolizzarlo).
Chitina: zucchero di struttura presente in alcuni animali (Gamberi, Aragoste).
LIPIDI (grassi):
- gruppo di sostanze organiche molto diverse fra loro. Hanno tutti stesse caratteristiche: 1) sono insolubili in solventi polari (acqua) perché sono apolari: essendo meno densi si dispongono in superficie. Agitando il miscuglio eterogeneo può succedere un emulsione (situazione temporanea in cui gocce di olio si disperdono nell'acqua).
2) sono le molecole organiche che liberano la maggio vcore quantità di energia chimica (producono il doppio dell'energia prodotta dai carboidrati) xché possiedono lunghi scheletri carboniosi saturati da atomi di idrogeno (molti legami carbonio-idrogeno). Hanno spesso il ruolo di messaggeri chimici fra interno e esterno cellula.
- 1 molecola di grasso (trigliceride) è idrofoba poiché è costituita x condensazione da 3 molecole di acido grasso (acido carbossilico caratterizzato da 1 lungo scheletro carbonioso) e 1 di glicerolo.
- acidi grassi: posson essere: - saturi: non compaiono doppi ma semplici legami fra atomi C e ogni atomo di C forma legami covalenti con altri 4 atomi e sue possibilità di legarsi sono esaurite. Consentono alle molecole di compattarsi le une con le altre e solidificare anche a temperatura ambiente (burro, grasso carne) - insaturi: compaiono doppi o tripli legami fra atomi C e ogni atomo di C non possiede il numero massimo di atomi di idrogeno che potrebbe avere. Consentono alle molecole di ripiegarsi rendendo + complessa disposizione molecole e tendono ad essere liquide a temperatura ambiente (olio). - polisaturi: molto resistenti ad alte temperature.
Gli acidi grassi insaturi posson essere idrogenati (saturati in un processo industriale con atomi di idrogeno: vengono rotti i doppi o tripli legami) divenendo simili a quelli saturi con consistenza solida.
Funzioni
1) come carboidrati (riserva energetica, realizzatori strutture cellulari, realizzatori nuove molecole biologiche)
2) copertura lipidica (mantenere temperatura corpo costante).
FOSFOLIPIDI E GLICOLIPIDI:
- sono costituiti da catene di acidi grassi attaccate ad uno scheletro di glicerolo.
Fosfolipidi: molecole lipidiche che costituiscono la struttura delle membrane cellulari. Sono polari e idrofili (posson reagire con l'acqua). 3° atomo di carbonio della
molecola di glicerolo non è collegato a un acido grasso, ma ad un gruppo fosfato (PO43-) carico negativamente a cui è legato un altro gruppo polare. Molecola: è
idrofila vicino a gruppo polare e idrofoba vicino a acidi grassi. Immersi in acqua tendono a andare in superficie avvicinandosi tra loro con le "teste" (idrofile e polari)
corrispondenti al gruppo fosfato rivolte verso l'acqua e "code" (idrofobe e apolari) costituite da acidi grassi rivolte verso l'interno in posizione opposta).
Nelle cellule essi tendono a formare doppi strati disponendosi con le code di acidi grassi le une contro le altre e teste contenenti fosfato rivolte verso ambiente esterno
acquoso.
Glicolipidi: 3° atomo di carbonio della molecola di glicerolo si lega a una catena corta di carboidrati (contiene da 1 a 15 monosaccaridi). La "testa" composta dal
carboidrato è idrofila e le code formate da acidi grassi sono idrofobe. Immersi in acqua si comportano come fosfolipidi.
Sono i componenti importanti delle cellulari.
CERE:
- lipidi strutturali (costituiscono un rivestimento protettivo e impermeabile del pelo piumaggio animali, pelle, esoscheletro insetti, sui frutti e foglie di piante)
- sono idrofobe e importanti x organismi che hanno necessità di non perdere acqua.
STEROIDI (come colesterolo):
- non hanno composizione chimica e struttura simile a altri lipidi ma appartengono a macromolecola dei lipidi xchè sono insolubili in acqua (idrofobe e apolari).
- hanno struttura formata da 4 anelli carboniosi fusi tra loro ed ad ogni estremità vi sono atomi di C e H.
- es: colesterolo: grasso prodotto dal fegato dei mammiferi a partire da acidi grassi saturi introdotti con l'alimentazione (carne, formaggio, tuorlo dell'uovo).
È importante x sintetizzare ormoni steroidi (cortisolo, estrogeni e testosterone). Elevati concentrazioni di esso nel sangue possono provocare la
aterosclerosi (accumulo colesterolo e altri grassi su pareti interne arterieà crescita anomala di tessuto fibroso e ostruzione vasi sanguignià
ischemia: incorretto trasporto sangue a 1 organo o tessutoà infarto o ictus).
PROTEINE:
- grosse molecole che contengono spesso centinaia di amminoacidi (piccole molecole organiche semplici disposte in sequenza che contengono azoto)
- molecole organiche + diffuse (+ 50% della maggior parte viventi è composto da proteine; non le piante: ne hanno poche xkè hanno tanta cellulosa).
FUNZIONI: 1) di trasporto (es: emoglobina: trasporta ossigeno)
2) strutturali: fanno parte di strutture cellulari (es: membrana cellulare)
3) ormonali (ormone: sostanza che permette ad un tessuto di lavorare)
4) di difesa immunitaria (anticorpi: proteine complesse e particolari che difendono il corpo)
5) di enzimi: catalizzatori delle reazioni chimiche (sostanze in grado di accelerare reazioni chimiche nelle cellule)
Es proteina: EMOGLOBINA: proteina sintetizzata e trasportata dai globuli rossi del sangue. Molecole: si posson legare facilmente con ossigeno preso dai polmoni e trasportato in tutto il corpo. La sua molecola presenta struttura quaternaria formata da 4 catene polipeptidiche con 150 amminoacidi ciascuna ed è ripiegata attorno a un gruppo contente ferro: eme (serve a tenere uniti i 4 legami terziari). Può capitare che molecole di emoglobina presentino anomalie funzionali: anemia falciforme: ossigeno si stacca e molecole cambiano forma combinandosi fra loro e formando strutture + rigide e di forma allungataà globuli rossi si induriscono e deformano e si rompono facilmente: se ostruiscono piccoli vasi sanguigni provocano grumi di sangue che impediscono corretto rifornimento di ossigeno a organià dolori o vita breve.
Emoglobina della cellula falciforme e emoglobina normale variano per presenza della valina al posto dell'acido glutamminico che fa allungare struttura dell'emoglobina a causa della esistenza di 2 regioni che attraggono le molecole circostanti. Anche 2 amminoacidi diversi su 600 può provocare la morte.
![]()
![]()
![]() AMMINOACIDI
AMMINOACIDI
- sono molecole organiche (monomeri che costituiscono i polimeri proteici) costituite da carbonio, idrogeno, ossigeno e azoto.
- sono 20 tipi in totale
STRUTTURA: ogni amminoacido ha 1 atomo di C al centro a cui si legano un gruppo amminico (NH2), un gruppo carbossilico (COOH) e un atomo di idrogeno.
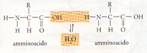
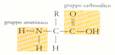 - i 20 amminoacidi esistenti differiscono
per gruppo R (radicale: occupa 4° legame covalente dell'atomo di C
centrale e possiede una struttura chimica diversa in ogni tipo di amminoacido,
quindi ciò determina diverse proprietà biologiche dei singoli
amminoacidi e quindi dei vari tipi di proteine). L'assemblamento di 2 o +
amminoacidi (attraverso una reazione di condensazione: in acqua) forma le
proteine: se amminoacidi legati sono 2, si forma un legame peptidico, quando sono + di 2 si forma un legame
polipeptide.
- i 20 amminoacidi esistenti differiscono
per gruppo R (radicale: occupa 4° legame covalente dell'atomo di C
centrale e possiede una struttura chimica diversa in ogni tipo di amminoacido,
quindi ciò determina diverse proprietà biologiche dei singoli
amminoacidi e quindi dei vari tipi di proteine). L'assemblamento di 2 o +
amminoacidi (attraverso una reazione di condensazione: in acqua) forma le
proteine: se amminoacidi legati sono 2, si forma un legame peptidico, quando sono + di 2 si forma un legame
polipeptide.
- 8 dei 20 amminoacidi sono detti essenziali: non possono essere sintetizzati xchè sono già costruiti e vengono introdotti nell'organismo attraverso gli alimenti.
Li troviamo negli animali ma non nei vegetali (eccetto la soia che li ha).
![]() Livelli di organizzazione
proteica:
Livelli di organizzazione
proteica:
- proteine: nelle cellule sono assemblate in lunghe catene polipeptidiche dove amminoacidi si susseguono uno dopo l'altro e sono flessibili con consistenza elastica.
STRUTTURA proteine: può essere primaria, secondaria, terziaria o quaternaria ma quest'ultime 3 dipendono dalla struttura primaria (sequenza lineare):
PRIMARIA: se sequenza di amminoacidi è lineare legati con legami peptidici; è caratteristica di ogni proteina e determina caratteristiche strutturali e funzione biologica.
SECONDARIA: formata da 2 strutture primarie: se sequenza di amminoacidi è ad elica (o a spirale), a foglio ripiegato o a forma di cavo; forma: ripiegata grazie a
legami idrogeno che si spezzano e riformano continuamente. Proteine elicoidali: hanno 1 forma a spirale e sono elastiche. Es: miosina (componente muscoli) e
cheratina (componente capelli). Proteine a foglio ripiegato non sono elastiche ma sono lisce e soffici. Proteine a forma di cavo: si avvolgono a 3 x volta l'una sull'altra x
formare 1 molecola simile a un cavo. Poi si raggruppano in lunghe e sottili fibrille. Es: collagene (componente cartilagine, ossa e tendini).
TERZIARIA: struttura che si forma come risultato di interazioni (attrazione o repulsione con gruppo R polare e repulsione tra gruppi R apolari e molecole d'acqua
circostanti) tra gruppi R degli amminoacidi che li compongono. È terziaria se sequenza è globulare (struttura secondaria: si ripiega su se stessa). Le proteine globulari
hanno sequenze di amminoacidi irregolari e complesse. Forma: tridimensionale. Gruppi che contengono zolfo posson formare legami covalenti fra loro (legami di ponti disolfuro: molto forti: collegano alcune parti delle molecole proteiche). Proteine globulari: trasportano enzimi.
QUATERNARIA: livello di organizzazione delle proteine che comporta l'interazione tra 2 o + polipeptidi. Proteine globulari: trasportano enzimi.
NUCLEOTIDI E ACIDI NUCLEICI:
ACIDI NUCLEICI: molecole che codificano l'informazione che dirige la sintesi dell'enorme varietà di molecole proteiche nelle cellule degli organismi viventi. In natura ne troviamo 2: acido ribonucleico (RNA: contiene ribosio) e acido deossiribonucleico (DNA: contiene deossiribosio)
NUCLEOTIDI: lunghe catene che costituiscono gli acidi nucleici. Ogni nucleodtide è formato da 3 parti: un gruppo fosfato (parte acida), uno zucchero con 5 atomi di carbonio (es: ribosio o deossiribosio) e una base azotata (in totale sono 5: adenina, citosina, meosina, . ) . Hanno funzione di trasportatori dell'energia per permettere reazioni chimiche che avvengono dentro cellule. La molecola + protagonista del trasporto dell'energia nella maggior parte dei processi è l'adenosina trifosfato (ATP o ATPosi se si tratta di un enzima). I prodotti della reazione + comune sono adenosina difosfato (ADP: costituita da energia e gruppo fosfato) e adenina monofosfato (AMP)
DNA: porta il messaggio genetico: contiene le informazioni organizzate in geni (unità ereditate dai genitori) che permettono l'assemblamento corretto di tutte le proteine seguendo la giusta sequenza.
RNA: è una copia del messaggio genetico portato da un pezzo di DNA che permette la sintesi proteica nel citoplasma della cellula.
![]()
BASI CHIMICHE DELL'EREDITARIETA':
Cromosoma eucariote: presenta l'ACIDO DEOSSIRIBONUCLEICO (DNA) e proteine (entrambi con ruolo di materiale genetico).
PROTEINE: polimeri di amminoacidi; DNA (polimero formato da 4 tipi diversi di nucleotidi).
DNA:
Friedrick Miescher: nel 1869 lo isolò e ne trasse una sostanza bianca, zuccherina, acida e contenente fosforo. Il DNA è costituito da nucleotidi che a suo volta sono composti ciascuno da una base azotata (ci sono 2 tipi: purine con struttura a 2 anelli come l'adenina e la guanina e pirimidine aventi 1 solo anello come citosina e timida) zucchero con 5 atomi di carbonio (pentoso: deossiribosio) e da 1 gruppo fosfato.
: Avery, dopo esperimenti su batteri, stabilì che il DNA fosse l'unico materiale genetico della cellula ma tale idea fu accantonata x anni xkè i batteri procarioti erano considerati organismi inferiori e xkè la molecola di DNA costituita da 4 nucleotidi sembrava troppo semplice x assolvere il compito complesso di portare l'informazione ereditaria.
: si eseguirono numerosi esperimenti impiegando come campioni i batteriofagi (virus che attaccano i batteri), costituiti da moltissimo DNA e proteine. Si cercò di capire quale dei 2 tipi di molecola contenesse i geni virali (materiale ereditario che dirige la sintesi di nuovi virus all'interno della cellula batterica).
: Hershey e Chase scoprirono che solamente il DNA dei batteriofagi era coinvolto nel processo di duplicazione e che le proteine non potevano costituire il materiale ereditario. Per giungere a tale informazione eseguirono un esperimento: presero 2 campioni separati di fagi (con il fosforo x il DNA e zolfo x le proteine) che iniettarono in 2 batteri uguali. Avvenne il contatto (inizio del ciclo infettivo), l'inoculazione (cuore ciclo infettivo), il mescolamento e la separazione x centrifugazione (x separare le cellule da ogni materiale virale rimasto fuori da esse). Furono esaminati i campioni di materiale x la ricerca della radioattività e quindi verificare la presenza o meno del virus all'interno del batterio. Scoprirono che l'isotopo radioattivo 35S era rimasto fuori dalle cellule batteriche mentre l'isotopo radioattivo 32P era entrato nelle cellule ad infettare il batterio. Le proteine sono quindi un contenitore del DNA dei batteriofagi. Il DNA entra nelle cellule portando il messaggio ereditario completo del virus ed è perciò in grado di dirigere la formazione di nuovo DNA virale e nuove proteine virali.
Alfred Mirsky: dimostrò che le cellule somatiche di qualsiasi specie contengono uguali quantità di DNA, mentre i gameti contengono esattamente la metà del DNA delle cellule somatiche.
Edward Chargaff: analizzò il contenuto in purine e pirimidine del DNA di molte specie di esseri viventi e stabilì che basi azotate non son sempre presenti in stesse quantità. La proporzione delle 4 basi azotate è la stessa in tutte le cellule di tutti gli individui della stessa specie ma è diversa in specie diverse.
MODELLO DI WATSON E CRICK:
: James WATSON e Francis CRICK: scienziati interessati al DNA e lavorarono insieme x risolvere il problema della struttura molecolare: organizzarono dati noti sul DNA e li organizzarono in modo logico: i dati noti erano: 1) La molecola del DNA era di grandi dimensioni, lunga e sottile ed era formata da nucleotidi contenti ciascuno una purina o pirimidina, il deossiribosio e un gruppo fosfato. 2) Pauling: le proteine sono disposte spesso in modo elicoidale grazie ai legami idrogeno che si formano adiacenti all'elica. 3) Che la struttura del DNA è simile a quella delle proteine (teoria: Pauling; conferma: Wilkins e Franklin). Chargaff: la proporzione dei nucleotidi di DNA contenenti timina e adenina, guanina e citosina è circa 1:1.
COSTRUZIONE DEL MODELLO:
Watson e Crick cercarono di costruire un modello di DNA partendo dai dati noti e in grado di spiegare il suo ruolo biologico.
1) DNA: conteneva molecole eterogenee e varie xkè trasportavano tante informazioni genetiche.
2) esiste una duplicazione rapida e precisa del DNA che produce copie fedeli del patrimonio ereditario da trasmettere nelle cellule di generazione in generazione.
3) DNA: è una doppia elica lunga e spiralizzata costituita da 2 montanti formati da molecole di zucchero alternate a gruppi fosfato e da numerosi pioli perpendicolari ai montanti costituiti da basi azotate ognuna formante un legame covalente con lo zucchero nel tratto di montante adiacente. Le basi azotate sono tenute unite da legami idrogeno e la distanza tra i 2 montanti è di 2 nanometri. I pioli devono sempre essere combinazioni di una purina con una pirimidina in modo che la molecola di DNA non presenti la stessa larghezza.
4) costruirono un modellino tridimensionale in stagno e ferro della molecola di DNAà scoprirono che i nucleotidi potevano essere disposti in qualunque ordine e che la struttura delle basi azotate permetteva solo gli appaiamenti tra adenina e timina con 2 legami idrogeno e tra guanina e citosina con 3 legami idrogeno. Le basi appaiate sono complementari.
STRUTTURA DNA di Chargaff:
Ogni filamento di DNA ha una direzione e presenta un legame tra un gruppo fosfato e una molecola di zucchero in posizione 5I (5° atomo di C dell'anello dello zucchero) e un'altra molecola di zucchero in posizione 3I (3° atomo di C dello zucchero). Ogni filamento ha 2 estremità: 5I (termina con gruppo fosfato) e 3I (termina con gruppo ossidrilico) e all'interno della doppia elica i 2 filamenti si muovono in senso opposto: l'estremità 5I si dirige verso l'estremità 3I in direzione opposta (filamenti antiparalleli).
DUPLICAZIONE DEL DNA:
- è un processo rapido che si verifica durante la fase S dell'interfase che precede mitosi o meiosi ed è il processo che comporta la duplicazione dei cromosomi.
- Mentre si duplicano i cromosomi, la molecola di DNA si apre lungo la linea mediana e le basi azotate appaiate si separano in corrispondenza di legami idrogeno.
- ciascuno dei 2 filamenti in divisione dirige la sintesi di un nuovo filamento complementare utilizzando i nucleotidi presenti nella cellula. Se sul vecchio filamento era
presente T, A prenderà posto nel nuovo filamento, mentre G si appaierà solo con C, . à ogni filamento forma 1 copia di quello a cui era appaiato originariamente e si
formano 2 copie identiche della molecola iniziale.
- deve avvenire in modo perfetto
- si dice semiconservativa quando viene costruita una nuova molecola di DNA che possiede 1 filamento originale della molecola madre e uno di nuova sintesi.
- necessita di un gran numero di diversi enzimi ognuno specifico nel catalizzare una particolare fase del processo.
MECCANISMO:
Per far avvenire la duplicazione del DNA, la doppia elica deve potersi svolgere e il DNA deve assumere la forma di scala a pioli. Ecco il meccanismo:
- La duplicazione inizia dal punto di origine della duplicazione (una specifica sequenza di nucleotidi) quando gli elicasi (enzimi) si dirigono al punto di origine e
inizian a spezzare i legami idrogeno tra le basi azotate complementari. Ciò favorisce l'apertura della doppia elica nella bolla di duplicazione (duplicazione:
bidirezionale: xkè si apre una bolla che si allunga all'insù e all'ingiù ed ai suoi vertici troviamo 2 forcelle di duplicazione: strutture a Y) e grazie all'intervento delle
proteine di attivazione, i 2 filamenti di nucleotidi restano rigidi. Poi interviene un 3° gruppo di enzimi (DNA-polimerasi) con compiti di: 1) leggere le sequenze di
nucleotidi sui 2 filamenti stampo e scegliere i nucleotidi complementari da associare. 2) PROOFREADING: correzione della letturaà garantisce precisa duplicazione
del DNA: I DNA-polimerasi devono individuare e correggere gli errori (es. l'aggiunta di un nucleotide non complementare e non in grado di formare il legame nel
filamento in costruzione à rimuovono i nucleotidi fino al nucleotide appaiato correttamente e li sostituiscono con nucleotidi complementari e quindi adeguati).
Nei procarioti è presente 1 solo punto di origine, negli eucarioti ve ne sono molti in ogni cromosoma: la duplicazione si verifica lungo i cromosomi lineari mentre la
bolla si espande nelle 2 direzioni e termina quando essa incontra una 2° bolla adiacente. Il cromosoma sarà duplicato quando tutte le bolle saranno fuse tra loro.
Oltre ai DNA-polimerasi esistono altri enzimi riparatori che controllano costantemente la doppia elica di DNA e ogni volta che incontrano una coppia di nucleotidi
non giustamente appaiata, tagliano nel punto dell'errore e sostituiscono il nucleotide sbagliato con uno complementare (correggono errori sfuggiti).
Alla fine si ottengono 2 molecole costituite ciascuna dal filamento della molecola madre e da uno di nuova sintesi (duplicazione semiconservativa).
La struttura del DNA può essere danneggiata e modificata da agenti esterni (raggi X, radiazioni ultraviolette, sostanze chimiche, . )à radiazioni UV: posson causare
la perdita di una purina o la formazione di legami covalenti tra pirimidine adiacenti e potrebbero quindi compromettere il dispositivo di correzione della letturaà lesioni
della pelleà tumori.
CAUSA DELLA DIVERSITA' DEGLI ESSERI VIVENTI:
Watson e Crick costruendo il famoso modellino di una molecola di DNA spiegarono in che modo tale molecola portasse informazioni genetiche: le informazioni sono scritte nella sequenza delle basi azotate. In un virus si trovano 5.000 basi appaiate, nei 46 cromosomi umani 6 miliardi. Ciò spiega la diversità dei viventi.
FRAMMENTI DI OKAZAKI E TELOMERI:
- 2 filamenti che compongono una molecola di DNA sono antiparalleli: se osservati in direzione da 5I a 3I si muovono l'uno nel senso opposto dell'altro quindi a una
delle 2 estremità di una doppia elica, un filamento presenterà l'estremità 5I e l'altro 3I.
OKAZAKI - filamento 5I e 3I (GUIDA): viene duplicato in modo continuo e la duplicazione si completa prima rispetto all'altro filamento.
- filamento 3I e 5I (IN RITARDO): viene duplicato in modo discontinuo (molecole DNA-polimerasi: leggono filamento a piccoli pezzi e sintetizzano il
filamento complementare a pezzetti (frammenti di Okazaki). Poi enzima DNA-ligosi provvederà a legare tutti i vari pezzi ad eccezione dell'ultimo
frammento di Okazaki nei cromosomi eucarioti che andrà persoà DNA: si accorcia di un pezzetto. Cellula si può bloccare se perde informazioni e rischia
di morireà ciò avviene raramente xkè l'ultimo pezzo di filamento è spesso un telomero.
TELOMERI segmenti di DNA che si ripetono corrispondenti a parti di DNA che non danno informazioni alla cellula e che posson essere persi senza danneggiare la
cellula. Negli esseri viventi ce ne posson essere fino a 200. Esiste anche un enzima in grado di risintetizzare il DNA telomerico perso durante duplicazione
e mantenere integri i cromosomi: telomerasi (permette la ricostruzione dei telomeri e quindi è il sistema delle cellule di mantenersi in vita perenni):
presente solo in alcune cellule (del midollo osseo, riproduttive e cancerose).
TUMORI - si sviluppano quando una cellula non è + in grado di comunicare con cellule circostanti e si riproduce quando e come le pare (cellula cancerosa).
- l'insorgenza avviene a causa della modifica dei geni responsabili delle comunicazioni cellulari che diventano ONTOGENI (geni alterati capaci di
determinare un tumore: costruisce in modo anomalo un'enzima riparatore). Il 90% delle cellule cancerose produce telomerasi (se venisse bloccato questo
enzima l'attività di tale cellula si bloccherebbe).
VERSO LA SCOPERTA DEL DNA:
1928: Fredrick Griffith: studiò il modo di poter combattere il batterio responsabile della polmonite (Streptococcus pneumonite) causa di numerose vittime.
Egli stabilì che gli pneumococchi (batteri) esistono in forma virulente (provocano malattia e presentano una capsula polisaccaridica) e non virulente (innocue e prive di capsula). In + esperimenti iniettò contemporaneamente in alcuni topi dei batteri virulenti morti e batteri vivi non virulentià topi morirono. Con un'autopsia scoprì batteri vivi capsulati e virulenti nei corpi dei topi morti e dedusse che anche i batteri virulenti morti possono trasmettere la virulenza a batteri vivi non patogeni (fenomeno detto TRASFORMAZIONE e provocato dal FATTORE TRASFORMANTE).
1943: Avery: dimostrò che il fattore trasformante era il DNA. Grazie al DNA isolato vengono trasmessi caratteri ereditari da un ceppo batterico a un altro simile.
NATURA DEL DNA:
1869: DNA: fu classificato da Miescher come sostanza nucleina (dei nuclei delle cellule), isolata bianca, zuccherina, leggermente acida e contenente fosforo. Poi fu chimata acido nucleico e successivamente acido deossiribonucleico (x distinguerlo dall'RNA: ribonucleico).
1914: Feulgen: scoprì che DNA presenta una somiglianza al colorante rosso fucsina ma non rivelò sua scoperta. 10 anni dopo la colorazione di Fulgen rivelò che DNA è presente in tutte le cellule ed è localizzato su cromosomi. Levene: dimostrò che DNA poteva essere scomposto in uno zucchero pentoso, in un gruppo fosfato e 4 basi azotate: adenina, guanina (purine), citosina e timina (pirimidine). Stabilì quindi che ogni base azotata è legata a 1 molecola di zucchero e che si lega a un gruppo fosfato formando un'unica molecola chiamata nucleotide.
CODICE GENETICO E SINTESI PROTEICA:
GENI E PROTEINE:
1940: biologi capirono che le attività biochimiche della cellula dipendono da differenti enzimi specifici. La specificità dei diversi enzimi era il risultato della loro struttura primaria (sequenza degli amminoacidi presenti nella molecola proteica).
George Beadle: formulò l'ipotesi che i diversi colori degli occhi osservati nei mutanti fossero il risultato della variazione. Poi riuscì a dimostrare la relazione tra mutazioni e perdita di funzionalità di specifici enzimi. Beadle e Tatum affermarono che il responsabile di un determinato enzima è il gene. Per enzima si intende una proteina ma non tutte le proteine sono enzimi (possono essere ormoni, proteine strutturali, proteine di membrana). Siccome tutte le proteine sono determinate da geni si parla di "un gene - una proteina". In seguito "un gene - una catena polipeptidica" perché le proteine sono formate da più di una catena polipeptidica.
STRUTTURA EMOGLOBINA:
- è formata da 4 catene polipeptidiche (2 alfa e 2 beta e ciascuna formata da 50 amminoacidi),
- Linus Pauling: pensò che le malattie umane riguardanti l'emoglobina (es: anemia falciforme) erano conseguenza della mutazione della struttura proteica della
molecola di emoglobina. Egli per provare la sua teoria si servì della elettroforesi (tecnica che permette di separare le molecole organiche spesso disciolte in
soluzione sottoponendole all'azione di un debole campo elettrico). Con questo provò quindi che una persona affetta da anemia falciforme sintetizza un tipo di
emoglobina differente rispetto a una persona sana. L'emoglobina normale ha una maggiore carica negativa e quindi rimane più vicina al polo positivo rispetto
all'emoglobina delle cellule falciformi. L'emoglobina presente nell'eterozigote presenta l'emoglobina proveniente da cellule sia normali che falciformi.
- la vera differenza tra le molecole di emoglobina normale e di emoglobina di cellule falciformi è costituita da 2 soli amminoacidi su 600.
DAL DNA alla PROTEINA: RUOLO DELL'RNA
- molecola DNA: codice che contiene le istruzioni per le strutture e le funzioni cellulari, e queste istruzioni sono eseguite dalle proteine.
- la sequenza lineare degli amminoacidi di una catena polipeptidica determina la struttura tridimensionale dell'intera proteina che a sua volta determina la funzione.
RNA (acido ribonucleico): sostanza chimicamente simile al DNA ma non uguale perché presenta 3 differenze: 1) i nucleotidi dell'RNA contengono il ribosio e non il
desossiribosio come zucchero. 2) la base azotata timina (nel DNA) corrisponde all'uracile (pirimidina, nell'RNA) ma entrambi si legano all'adenina. 3) la maggior parte
dell'RNA è composto da un filamento singolo. L'RNA possiede un ruolo importante nella traduzione dell'informazione genetica (processo che traduce i segmenti di
DNA in sequenze di amminoacidi). Le cellule che sintetizzano grandi quantità di proteine sono ricche di RNA; nelle cellule eucariote l'RNA si trova nel citosol (luogo
dove avviene la sintesi proteica); le cellule procariote e eucariote in grado di produrre grandi quantità di proteine hanno numerosi ribosomi (ricchi di RNA).
- Anch'esso contiene informazioni sulla struttura proteica.
- esistono 3 tipi di RNA che agiscono come intermediari nei processi che portano alle proteine partendo dal DNA: messaggero,
RNA MESSAGGERO:
- le molecole di mRNA sono copie di sequenze nucleotidiche codificate nel DNA e sono costruite da un solo filamento. Ogni nuova molecola di mRNA viene copiata da uno dei 2 filamenti
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta