| chimica |
|
|||||
|
DETERMINAZIONE SPETTROFOTOMETRICA DEL FERRO NELL'ACQUA
- Scopo dell'esperienza sarà determinare, tramite spettrofotometria, la concentrazione dell'elemento ferro presente in una soluzione a titolo incognito. Per far ciò ci avvarremo dello spettrofotometro, strumento in grado di rilevare lo spettro elettromagnetico di assorbimento di un campione della sostanza in esame.
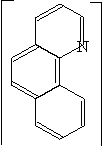
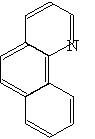
- Tale tipo di analisi colorimetriche richiede, appunto, l'utilizzo di sostanze colorate; Il ferro non possiede questo requisito e per poterlo analizzare tramite spettrofotometria è necessario usarne un derivato colorato, che rappresenti quantitativamente tutto il ferro in soluzione. Per ottenere ciò utilizzeremo la 1,10 fenantrolina (Phen), un legante bidentato contenente due atomi di azoto agenti da base e quindi in grado di legare doppiamente un atomo di ferro; Tale atomo formerà un complesso esacoordinato legando tre molecole di Phen, ognuna con due legami a "tenaglia" tipici dei chelanti, assumendo una struttura globale ottaedrica.
![]()
![]() 3 + Fe2+
→ Fe2+
3 + Fe2+
→ Fe2+
N N
![]()
![]()
- Tale complesso, oltre che stabile, possiede una spiccata colorazione rosso/arancio che lo rende perfetto per analisi spettrofotometriche. Il ferro possiede infatti conurazione elettronica esterna 3d6 con 6 elettroni sugli orbitali degeneri d; a seguito della formazione del complesso tale uniformità energetica degli orbitali viene rimossa, in particolare con la destabilizzazione da parte della fenantrolina degli orbitali dx2y2 e dz2. Gli altri tre orbitali d (dxy, dxz e dyz) non risentono invece della formazione del complesso, rimanendo a un livello di energia minore, mentre i succitati orbitali destabilizzati si posizionano a un livello di energia superiore. Per il principio di Afbau gli elettroni vanno a posizionarsi tutti sui tre orbitali a livello energetico inferiore ma tra i due livelli energetici degli orbitali viene a crearsi un gap tale che, a seguito di "salti" di elettroni dovuti a interventi esterni (quale può essere una radiazione elettromagnetica) il dislivello energetico è tale da provocare variazioni dello spettro elettromagnetico nel visibile.
dx2-y2,
dz2
![]()
h∙c
|
d
![]()
- Ottenuto così un complesso ben rilevabile, cerchiamo di capire quale possa essere il nesso tra tale analisi e la determinazione della concentrazione dell'elemento in esame in una certa soluzione. L'elemento in grado di rendere possibile questo è appunto lo spettrofotometro, nelle sue due modalità di analisi: quantitativa e qualitativa.
-Lo spettrofotometro è sostanzialmente formato da una sequenza di elementi: una sorgente di luce policromatica converge in un monocromatore (a reticolo o a prisma) che produce un fascio monocromatico dalla luce bianca di partenza. Tale fascio di luce attraversa una cella contenente il campione di sostanze in esame con una certa intensità luminosa I0 detta luce incidente; qui una parte della luce viene assorbita dalla sostanza e dalla cella portacampione esce luce con una certa intensità I, definita trasmessa. A sua volta tale fascio di luce viene convogliato in un rivelatore (che converte i fotoni in segnali elettrici, quantificandoli) e di lì in un registratore che archivia tali dati.
Fra tali intensità vi è ovviamente un rapporto del tipo I<I0 c con tali valori coincidenti nel caso limite in cui la sostanza non assorba su nessuna lunghezza d'onda.
- La modalità di misura qualitativa è effettuata facendo selezionare al monocromatore, in un intervallo da noi impostato, tutte le possibili lunghezze d'onda della luce incidente e di volta in volta registrare l'assorbanza a tale λ. Quello che otteniamo è lo spettro di assorbimento, un grafico relazionante assorbenza e lunghezza d'onda incidente specifico e identificante per ogni sostanza e dal quale è ricavabile un certo valore di picco, cioè la λ a cui l'assorbanza è massima.
- La misura quantitativa della luce "trattenuta" dal campione è come detto tale assorbanza, ricavabile dai dati di intensità di luce incidente e trasmessa secondo tali formule (T indica la trasmittanza):
|
|
|
|
|
- A sua volta, tale valore dell'assorbanza è esprimibile, tramite la legge di Lambert-Beer, come
A = ε x b x C
- In tale formula b rappresenta il cammino ottico, che nello strumento è fisso ed è dato dallo spessore del contenitore, detto cuvetta, che ospita il campione in esame; ε rappresenta invece il coefficiente di estinzione molare, specifico e considerato costante per una data sostanza ad una data lunghezza d'onda, benché possa subire lievi variazioni con la temperatura. La relazione tra assorbanza registrata dallo strumento e il parametro C della formula, cioè della concentrazione molare, è quindi diretta e utilizzabile per effettuare misure quantitative.
- Impostando una lunghezza d'onda fissa (preferibilmente quella per cui vi è un massimo di assorbimento, individuata tramite analisi qualitativa dello spettro come detto sopra) e registrando l'assorbanza di soluzioni a titolo vario è possibile costruire quella che viene definita retta di taratura; Un grafico relazionante assorbenza e concentrazione della sostanza in esame che, una volta realizzato in forma di retta, permetterà di risalire dall'assorbanza rilevata alla concentrazione della sostanza con ottima approssimazione, che è appunto il metodo che utilizzeremo per determinare la concentrazione di ferro in una soluzione a titolo incognito come prefisso nello scopo dell'esperienza.
PREPARAZIONE
- Il ferro che useremo sarà presente in soluzione sotto forma di solfato ammonico ferroso esaidrato (NH4)2Fe(SO4)2 · 6 H2O, con il ferro presente in uno stato di ossidazione +2. La solubilizzazione di tale sale in acqua sarà coadiuvata dall'aggiunta di acido solforico e a tutta una serie di "precauzioni" chimiche che rendano possibile la reazione:
- Il ferro deve rimanere nello stato di ossidazione +2 e non ossidarsi a ferro +3 per mezzo dell'ossigeno dell'aria; Anche il ferro ossidato forma un complesso con il Phen ma i due complessi non hanno lo stesso spettro di assorbimento e ciò porterebbe a confusione. Per ovviare a tale inconveniente si aggiunge alla soluzione un agente riducente, il cloridrato di idrossilammina NH2OH ∙ ∙HCl, che garantisce l'ossidazione costante allo stato +2 del ferro in soluzione. Tale sostanza viene utilizzata preparandone una soluzione da 10g in 100ml di acqua distillata.
- Anche il pH deve essere tenuto sotto controllo: per valori troppo acidi (pH<3) gli N della fenantrolina vengono protonati, impedendone la formazione del complesso con il ferro; all'opposto, valori troppo basici (pH>9) farebbero precipitare il ferro sotto forma di idrossido con una reazione del tipo à Fe2+ + 2OH- → Fe(OH)2↓
- Il problema del pH viene risolto aggiungendo alla soluzione dell'acetato di sodio CH3COONa, anch'esso preparato tramite 10g in 100ml di acqua distillata; Unito alla soluzione campione, l'acetato di sodio si dissocerà e, reagendo con gli ioni liberati dalla dissociazione dell'acido solforico, andrà a riformare dell'acido acetico CH3COOH. Si verrà così a creare in soluzione un sistema tampone, che garantirà un pH compreso tra 3 e 9 ottimale per lo svolgimento dell'esperienza.
- Per poter costruire una retta di taratura efficace utilizziamo cinque soluzioni preparate miscelando opportunamente quanto indicato sopra e addizionando la 1,10 fenantrolina (preparata sciogliendo 0,25g di questa sostanza in 100ml di acqua) in largo eccesso per essere sicuri di legare completamente tutto il ferro presente; tali soluzioni, a concentrazione nota, ci permetteranno di graficare il rapporto assorbenza/concentrazione. La preparazione delle soluzioni è stata effettuata aggiungendo rispettivamente 0, 10, 20, 25, 35 ml di soluzione della sostanza madre, precedentemente preparata disciogliendo, all'interno di un matraccio da 500ml, 0,35g del sale ferroso con acqua distillata; dopo aver portato a volume, erano stati aggiunti 12,5ml di H2SO4, travasando infine 50 ml del liquido in un altro matraccio da 500ml, diluiti poi con acqua distillata.
- In ognuno dei sei matracci, sono stati in seguito aggiunti, oltre che 5ml di fenantrolina, 1ml di cloridrato di idrossilammina e 5ml di acetato di sodio. La soluzione a cui non abbiamo aggiunto la sostanza madre è detta "bianco"; questo indica una soluzione che sia esattamente uguale a quella campione, con l'unica differenza di non presentare disciolta la sostanza di cui si vuole rilevare l'assorbanza. Come è intuibile, tale stratagemma permette di ignorare eventuali percentuali di assorbenza dovuta non al ferro ma ad altre delle sostanze presenti in soluzione. L'introduzione del bianco inoltre evita di includere eventuali errori nella determinazione della concentrazione della specie chimica in esame dovuti a numerosi fattori non legati alla concentrazione stessa, come l'assorbimento da parte delle pareti della celletta, la rifrazione o la riflessione.
ESECUZIONE
- Per prima cosa tariamo lo strumento, utilizzando il succitato bianco per indicare allo spettrofotometro quale sia la quantità di assorbanza da "ignorare", azzerandolo. Sia il bianco sia tutti gli altri campioni vengono inseriti nello strumento dentro speciali contenitori detti cuvette, delle provette in plastica sagomate come dei parallelepipedi che presentano due facce zigrinate per la presa e due facce lisce, da non toccare per non sporcarne la superficie, che rappresentano la zona dove passeranno i fasci luminosi (cammino ottico di 1cm).
- Dopo tale operazione prendiamo una qualsiasi delle soluzioni a diversa concentrazione preparate e ne eseguiamo un'analisi qualitativa, andando a indicare un range di osservazione dell'assorbanza compreso tra 450 e 600nm; tale primo grafico rappresenta lo spettro specifico della sostanza in esame, e ci è utile per individuare il picco di assorbanza.
PICCO D'ASSORBIMENTO: 510nm ABS: 0.684
- Individuato un massimo di assorbanza a una lunghezza d'onda λ di 510nm, reimpostiamo lo spettrofotometro predisponendolo per un'analisi non più qualitativa ma quantitativa proprio su tale lunghezza d'onda. Disponiamo ora nello strumento le 5 cuvette in ordine di concentrazione crescente, includendo oltre alle 4 soluzioni a concentrazione nota il bianco iniziale; lo strumento registra l'assorbanza relativa a ogni differente concentrazione e, utilizzando il metodo dei minimi quadrati, estrapola da tale rapporto un grafico che mostra il crescere dell'assorbanza al crescere della concentrazione.
|
Soluzione |
Concentrazione (mM) |
ABS |
λ (nm) |
|
BIANCO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Sfruttando tale grafico possiamo ora procedere alla determinazione spettrofotometrica vera e propria: prendiamo una soluzione precedentemente preparata sempre della stessa sostanza ma stavolta a titolo incognito e ne registriamo il valore di assorbanza alla lunghezza d'onda trovata di 510nm, rilevando un valore di ABS pari a 0.334; Posizionando tale valore sul grafico troviamo che a tale assorbanza e a condizione di λ e temperatura fissa la concentrazione della soluzione analizzata è circa 0.0288mM.
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta