| chimica |
|
|
|
 OBIETTIVI:
OBIETTIVI:
Verificare come varia la velocità di reazione in funzione alla concentrazione.
Verificare come varia la velocità di reazione in funzione alla temperatura.
|
Fattori che influenzano la velocità delle reazioni: Aumento di temperatura. Aumento della concentrazione dei reagenti. Aumento della suddivisione dei reagenti, ossia della superficie di contatto tra i reagenti. Catalizzatori: - organici (enzimi). - inorganici. Rapporto
di diluizione: |
OCCORRENTE:
Materiali
Cinque becher da: 50ml, 100ml x3, 150ml.
Propipetta.
Due pipette graduate da: 5ml, 10ml.
Piastra riscaldante.
Provette e portaprovette.
Cilindri graduati da: 5ml, 100ml
Spruzzetta.
Pinza per provette.
Bagno maria.
Ancorette magnetiche: quattro piccole e una grande.
Bacchetta di vetro a punta angolata.
Termometro.
Cronometro.
Disco di carta bianca.
Pipetta di Pasteur.
Sostanze
Permanganato di potassio KMnO4.
Acido ossalico H2C2O4.
Acido solforico H2SO4.
Acqua distillata H2O.
DESCRIZIONE DELL'ESPERIENZA:
Prima fase:
In ogni becher vanno messi 10ml di permanganato di potassio KMnO4 N/20 (normal ventesimo), che si presenta di colore viola intenso. Per prelevare il liquido ci si può aiutare con la pipetta di Pasteur, alla cui estremità è fissata la propipetta.
Prelevare 5ml di acido solforico H2SO4 con la pipetta di Pasteur misurandoli nel cilindro graduato; metterli poi in ognuno dei quattro becher già contenenti KMnO4.
Aggiungere in ogni becher le seguenti quantità di acqua distillata:
nel primo à 0ml.
nel secondo à 20ml.
nel terzo à 40ml.
nel quarto à 60ml.
La capacità d'acqua va misurata nel cilindro graduato con capacità di 100ml.

posizionare il disco di carta sulla piastra e a turno i quattro becher, ciascuno contenente un'ancoretta magnetica, per rendere omogenea la soluzione; posizionare la velocità del rotore sul livello 2.
prelevare con la pipetta di Pasteur 40ml di acido ossalico H2C2O4 (10ml x 4 volte) e metterli in un solo becher vuoto.
Far partire il cronometro non appena l'acido ossalico viene versato nel becher contenente permanganato di potassio, acido solforico e acqua, e fermarlo nel momento in cui il liquido nel becher sarà del tutto incolore. Ripetere l'operazione per tutti e quattro i becher preparati come sopra.
|
|
10ml di KMnO4 |
5ml di H2SO4 |
0ml di H2O |
10ml di H2C2O4 |
|
|
|
10ml di KMnO4 |
5ml di H2SO4 |
20ml di H2O |
10ml di H2C2O4 |
|
|
|
10ml di KMnO4 |
5ml di H2SO4 |
40ml di H2O |
10ml di H2C2O4 |
|
|
|
10ml di KMnO4 |
5ml di H2SO4 |
60ml di H2O |
10ml di H2C2O4 |
|
OSSERVAZIONI: assisto ad una scala cromatica, indice del processo di reazione che sta avvenendo, e risulta concluso quando si raggiunge il liquido incolore.
Viola - rosso - arancio - giallo - incolore.
NB: l'acido solforico non va considerato, perché funge solo da catalizzatore: la reazione, infatti, avviene solo tra il permanganato di potassio e l'acido ossalico.
1° becher: rapporto diluizione = 1
2° ' : ' ' = ![]()
3° ' : ' ' = 0,2
4° ' : ' ' = 0,142
Seconda fase:
Preparare sulla piastra riscaldante il bagno maria, azionare il rotore a velocità 3 o 4 e alzare la temperatura (heating) fino a 100-l50°C: la spia luminosa si spegnerà non appena la piastra avrà raggiunto la temperatura impostata. Tuttavia la temperatura andrà controllata anche all'interno del bagno maria mediante il termometro.
Preparazione delle provette: in quattro provette, servendosi della pipetta di Pasteur, versare 5ml di permanganato di potassio e 2ml di acido solforico, misurati col cilindro graduato di capacità 5ml; in altre quattro provette versare 5ml di acido ossalico. Sistemarle poi tutte nel portaprovette.
Quando la temperatura al termometro raggiunge i 27°C, immergere, servendosi della pinza di legno per provette, la provetta contenente 5ml di permanganato di potassio e 2ml di acido solforico e la provetta contenente 5ml di acido ossalico.
Aspettare uno o due minuti in modo da rendere omogenea la temperatura in entrambe le provette.
Versare l'acido ossalico nel permanganato di sodio e contemporaneamente far partire il cronometro, per misurare il tempo di decolorazione; mescolare continuamente con la bacchetta angolata, girandola con due dita.
Ripetere l'operazione con le altre tre provette, variando la temperatura a intervalli regolari:
27°C, 37°C, 47°C, 57°C.
|
|
5ml KMnO4 + 2ml H2SO4 + 5ml H2C2O4 |
27°C |
|
|
5ml KMnO4 + 2ml H2SO4 + 5ml H2C2O4 |
37°C |
|
|
|
5ml KMnO4 + 2ml H2SO4 + 5ml H2C2O4 |
47°C |
|
|
|
5ml KMnO4 + 2ml H2SO4 + 5ml H2C2O4 |
57°C |
|
NB: la temperatura massima è 60°C, poiché l'acido ossalico, superata tale temperatura, si dissocia spontaneamente, perdendo le sue caratteristiche di reattivo.
Raggiunta la temperatura voluta, si consiglia di spostare il bagno maria dalla piastra riscaldante per non farla aumentare ulteriormente.
CONCLUSIONI:
Prima fase: le diverse quantità di acqua aggiunte nei becher servono a diluire le soluzioni in modo da far diminuire la concentrazione e 'l'attività' dei reagenti; ciò è stato provato dal fatto che più la soluzione è diluita (e quindi minore la concentrazione), maggiore è il tempo di decolorazione.
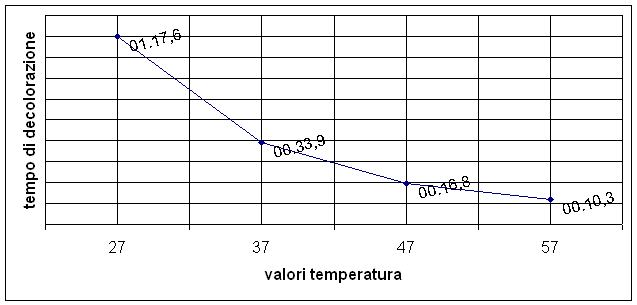
Seconda fase: abbiamo provato anche che il fattore temperatura influenza la velocità delle reazioni chimiche: infatti, maggiore è la temperatura, minore è il tempo di decolorazione, indice di avvenuta reazione.
Le grandezze sono
inversamente proporzionali, infatti, dal grafico si può notare che danno
origine ad un ramo di iperbole equilatera ![]() .
.
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta