| chimica |
|
LA LEGGE PERIODICA
Le proprietà chimiche e fisiche degli elementi sono una funzione periodica del numero atomico.
RAGGIO ATOMICO
Metà della distanza minima di avvicinamento tra gli atomi di una sostanza elementare. Diminuisce lungo il periodo, da sinistra a destra; aumenta scendendo lungo il gruppo
ELETTRONEGATIVITA'
L'andamento dell'elettronegatività sulla tavola periodica è il seguente:
cresce, lungo un periodo, da sinistra verso destra, e, lungo un gruppo,
dal basso verso l'alto.
ENERGIA DI IONIZZAZIONE
Quantità di energia necessaria ad allontanare l'elettrone più esterno da un atomo gassoso formando uno ione +1. Aumenta nel periodo da sinistra a destra Diminuisce scendendo lungo il gruppo.
ORBITALI NEI PRIMI TRE LIVELLI
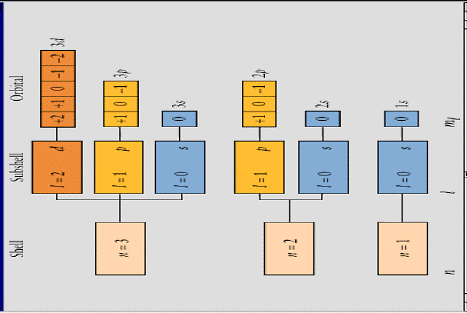
LA TAVOLA PERIODICA DEGLI ELEMENTI
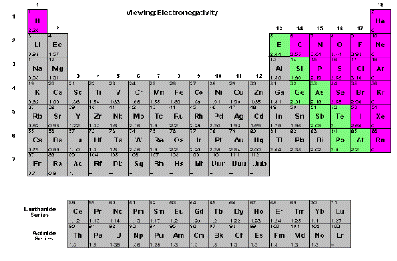
Conurazioni elettroniche degli atomi
Elenco degli orbitali occupati in un atomo nel suo stato fondamentale (ground state) di minor energia.
L'ordine dei livelli energetici degli
Orbitali Teoricamente
1s<2s<2p<3s<3p <3d <4s<4p<5s<4d
In pratica
1s<2s<2p<3s<3p<4s<3d
Il principio di esclusione di Pauli
. Un orbitale può contenere un massimo di due elettroni. Ed essi devono avere spin opposto.
. Elettroni appaiati con spin opposto creano campi magnetici nulli - ed atomi con elettroni spaiati creano campi magnetici
AUFBAU: (costruzione)
. Regole:
. 1. L'elettrone occupa l'orbitale a più bassa energia disponibile
. 2. Principio di Pauli: un orbitale può essere vuoto oppure occupato da un massimo di due elettroni. Due elettroni che occupano lo stesso orbitale hanno spin antiparallelo.
. 3. Principio di Hund: il riempimento di un orbitale degenere (stessa energia) si ha soltanto se gli altri orbitali degeneri sono già occupati da un elettrone
Modi di rappresentazione delle conurazioni elettroniche
Esempio del Calcio
(Ca, Z=20)
. Spettroscopico
1s2, 2s2p6,3s2p6,4s2
. Gas nobili
[Ar]4s2
Tabella periodica
. Lo schema complessivo della tavola periodica fu scoperto dal chimico russo Mendeleev nel 1869 che dispose gli elementi in gruppi e periodi in ordine di peso atomico.
. La tavola periodica è divisa in blocchi, dall'ultimo sottolivello occupato in base al principio di Aufbau. Gli elementi appartenenti ai blocchi s e p sono detti elementi dei gruppi principali.
. Il numero del periodo di un elemento corrisponde al numero quantico principale del guscio di valenza dei suoi elettroni.
. Il numero del gruppo corrisponde alla somma dei numeri degli elettroni s e p presenti nel guscio di valenza. Tutti i membri dello stesso gruppo hanno la stessa conurazione di valenza (con valori differenti di n).
Tabella periodica: i blocchi. Ultimo sottolivello occupato in base al principio di Aufbau: blocco s, blocco d, blocco p

Tabella Periodica: i gruppi e i periodi
Periodi Gruppi![]()
![]()
![]()
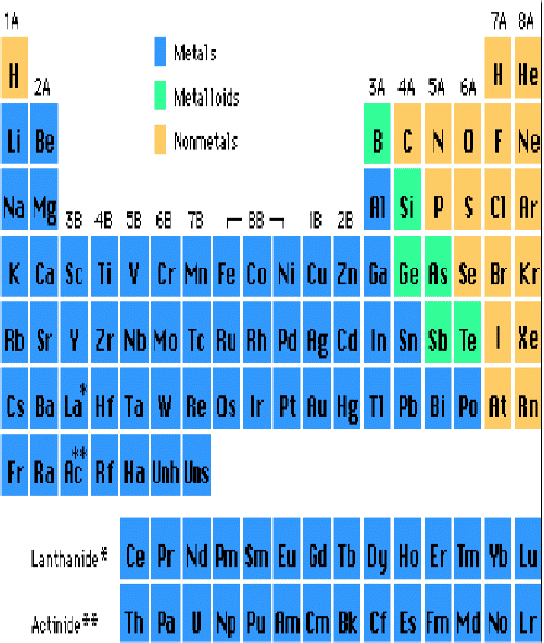
Periodicità delle proprietà
Le proprietà degli elementi mostrano una sorprendente periodicità.
. Dimensioni degli atomi
. energia di ionizzazione
. affinità elettronica
. elettronegatività.
Dimensioni degli atomi
Raggi atomici: come definire il raggio di
un atomo.
. Il raggio atomico diminuisce nel periodo da sinistra verso destra ed
aumenta nel gruppo dall'alto verso il basso
. La diminuzione che si osserva nell'ambito di un periodo, per esempio
dal Li al Ne, è il risultato dell'aumento delle attrazioni del nucleo
. L'aumento all'interno di un gruppo, per esempio dal Li al Cs, è perchè gli elettroni più esterni occupano livelli che sempre più lontani dal nucleo.
.L'energia di ionizzazione è l'energa che si deve fornire all'atomo per strappare un elettrone
.Aumenta spostandosi verso destra e verso l'alto nella tavola periodica degli elementi.
. Aumenta nel un periodo atomi diventano più piccoli, sono più vicini ad un nucleo più fortemente carico
. Diminuisce nel perché l'elettrone più esterno e' distante dal nucleo
. Le basse energie di ionizzazione giustificano il carattere metallico,
Affinità elettronica.
. l'energia liberata quando un atomo neutro viene addizionato di un elettrone
(formazione di anione):
E(g) + e- E-(g) + AF
. Si dice che un elemento ha una elevata affinità elettronica forma un anione in modo esortermico, entalpia negativa,
. i valori più alti si riscontrano in prossimità del fluoro
ELETTRONEGATIVITA'
|
ENERGIA DI IONIZZAZIONE |
AFFINITA' ELETTRONICA |
COMPORTAMENTO |
|
BASSA |
BASSA |
CATIONI |
|
ALTA |
ALTA |
ANIONI |
elettronegatività χ (la lettera greca chi), definita come
(energia di ionizzazione + affinità elettronica)/2
|
ELETTRONEGATIVITA' |
COMPORTAMENTO |
|
BASSA |
ALTA |
Conurazioni elettroniche degli ioni
. I cationi (ioni con carica +) si formano togliendo elettroni dagli orbitali a maggior energia (esterni)
. Gli anioni (-) aggiungendo elettroni agli orbitali disponibili a minore energia
Gli elementi del blocco d
. sono metalli di transizione. Quelli che si trovano a destra, come il rame e l'oro, sono meno reattivi. Le proprietà degli elementi del blocco d sono intermedie, o di transizione, tra quelle degli elementi del blocco s e quelle
degli elementi del blocco p; da qui l'origine del loro nome comune, «metalli di transizione».
. la capacità che molti di essi presentano di formare più cationi di carica differente. Il ferro, forma ioni ferro(II) e ferro (III), rame forma ioni rame(I) e rame(II),
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta