| chimica |
|
|||||
|
IDROLISI.
Allo stato solido i sali hanno dei reticoli di tipo ionico; tutti i sali, pertanto, con pochissime eccezioni, sono elettroliti forti. Quando sciogliamo un sale in acqua, gli ioni si legano a un certo numero di molecole di acqua (si idratano) e acquistano la possibilità di muoversi l'uno rispetto all'altro. Le interazioni di molti ioni con l'acqua si limitano al processo di idratazione, mentre molti altri ioni reagiscono con l'acqua secondo delle vere e proprie reazioni acido-base, alterando il rapporto molare tra [H+] e [OH-], che altrimenti sarebbe 1 a 1. Questa reazione è chiamata idrolisi dei sali. L'effetto dell'idrolisi è che la soluzione assume un pH che è maggiore o minore di 7, e generalmente questo effetto è causato solo da uno degli ioni formati dal sale. La reazione di uno ione specifico con l'acqua, in grado di influenzare il pH, è definita come la reazione di idrolisi dello ione stesso.
Per determinare se il sale si idrolizza, dobbiamo esaminare entrambi gli ioni del sale e domandarci se sono in grado di reagire con l'acqua per formare H+ o OH-. È qui che è opportuno considerare gli acidi e le basi che hanno originato il sale.
Sali di acidi forti e basi forti. Come regola generale, si può affermare che i sali formati da una acido forte e una base forte non danno idrolisi in soluzione.
Sali di acidi deboli e basi forti. Come regola generale, si può affermare che una soluzione di un sale formato dalla reazione di un acido debole con una base forte sarà basica a causa dell'idrolisi dell'anione (la base coniugata dell'acido debole).
Sali di acidi forti e basi deboli. Come regola generale, si può affermare che una soluzione di un sale formato dalla reazione di un acido forte con una base debole sarà acida a causa dell'idrolisi del catione (l'acido coniugato della base debole).
Sali di acidi deboli e basi forti. I sali che appartengono a questa categoria possono, oppure no, influenzare il pH della soluzione. Sia il catione sia l'anione presenti hanno la tendenza a idrolizzare, ma l'effetto che il sale ha sul pH dipende dalla capacità del catione di generare H+, rispetto a quella dell'anione di generare OH-.
La costante di equilibrio della reazione di idrolisi è detta costante di idrolisi Ki e si può facilmente mostrare che essa è legata al prodotto ionico dell'acqua ed alla costante di ionizzazione del sale che si è dissociato, secondo la relazione:
![]()
Per mostrare tale relazione, consideriamo due esempi:
Dalla dissociazione di NaF in acqua si liberano ioni Na+ e F-; Na+ non determina idrolisi; F-, base abbastanza forte, reagisce con H2O secondo l'equazione:
![]()
mettendosi in equilibrio con l'acido debole HF e rendendo basica la soluzione. Tale reazione rappresenta l'idrolisi dello ione F-.
Si dimostra che la costante di equilibrio della suddetta equazione, detta costante di idrolisi, è data da:
![]()
in quanto la reazione può essere considerata somma delle due equazioni:

In seguito alla dissociazione in acqua di NH4Cl, lo ione Cl- non si idrolizza, mentre lo ione NH4+, essendo un acido abbastanza forte, si idrolizza secondo l'equazione:
![]()
mettendosi in equilibrio con la sua base coniugata NH3 e rendendo acida la soluzione.
La costante di idrolisi di NH4+ è:
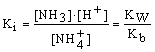
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta