| ricerche |
|
|||||
|
La DISTILLAZIONE.
Distillazione, operazione fisica di separazione dei componenti di una miscela omogenea (formata da due o più liquidi contenente un solido disciolto), basata sul fatto che i vapori che si liberano portando all'ebolizione tale miscela sono prevalentemente formati dal componente che presenta la temperatura di ebolizione inferiore e che in tal modo puo essere isolato (per condensazione) e raccolto, costituendo il distillato.
La distillazione si effettua in apposite apparecchiature (DISTILLATORI) che, nella forma piu semplice, sono costituiti da un recipiente(alambicco) nel quale bolle il liquido: il vapore che si sviluppa defluisce in un condensatore (solitamente di un serpentino), raffreddato esternamente da una circolazione di acqua fredda, in cui si trasforma in liquido che si raccoglie in un recipiente.
Dal punto di vista industriale la distillazione si effettua solitamente in impianti a forma cilindrica (colonne), suddivise internamente da diaframmi, detti piatti; sul fondo della colonna si somministra il calore che porta all'ebolizione la miscela, producendo dei vapori che, passando attraverso i vari piatti, vanno verso la parte alta, detta testa; poiché detti vapori si distanziano dalla sorgente di calore, in parte ricondensano e ricadono nuovamente verso il basso.
Questo successivo frazionamento fa si che i vapori che raggiungono la testa della colonna senza condensare siano costituiti praticamente dai componenti piu volatili, mentre la parte liquida che riamane nella coda sia costituita dai componenti meno volatili.
I vapori di testa vengono poi condensati e separati.
Tale metodo di distillazione prende il npme di RETTIFICA ed è utilizzato in tanti settori dell'industria chimica, come nel frazionamento del petrolio per ottenere i diversi combustibili da esso derivatooi, oppure per produrre i distillati alcolici.
Esistono tre tipi di distillazione usati da noi in laboratorio:
DISTILLAZIONE SEMPLICE;
DISTILLAZIONE FRAZIONATA;
DISTILLAZIONE IN CORRENTE DI VAPORE.
La distillazione semplice serve soprattutto per la separazione di due componenti con pinti di ebolizione molto differenti tra loro.
La distillazione frazionata viene utlizzata per la separazione di due componenti che hanno un punto di fusione molto vicino.
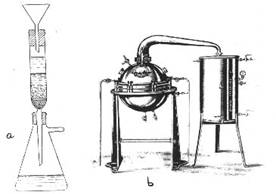
Il sistema della distillazione in corrente di vapore è costituito da varie parti,
la caldaia,che contiene l'acqua per il vapore di distillazione; la canna barometrica,essa pesca all'interno dell'acqua nella caldaia, e serve per regolarizzare la pressione all'interno della caldaia stessa; da un tubo di vetro, che ha la funzione di convogliare il vapore della caldaia nel gorgogliatore; il gorgogliatore, il vapore fuori esce dai fori e va a strappare gli oli essenziali all'interno del miscuglio; il pallone, che contiene il miscuglio da distillare; il riscaldatore, che utilizziamo per riscaldare il paollone; ed in fine il tubo refrigerante, dove viene condensata l'olio estratto.
SCOPO: Distillare l'acqua e tutti gli alcoli presenti nel vino dalla parte colorata.
Componenti da separare e loro punti di ebollizione:
ALCOL ETILICO 78°C
ALCOL METILICO 64°C
ALCOL PROPILICO E ISOBUTILICO 97°C
ALCOL AMILICO E ISOAMILICO 130°C
ACQUA 100°C
REAGENTE
Vino CANNONAU DI SARDEGNA (13% VOL.)
MATERIALE
Distillatore
Pallone di vetro
Ebollitori
Raccordo a tre vie (o a T)
Elevatore
Cilindro graduato (sensibilità 1ml ; portata 25 ml)
2 imbuti

PROCEDIMENTO
Inserire la miscela da distillare nel pallone con gli appostiti ebollitori (piccole palline di vetro o piccoli pezzetti di cermica che hanno lo scopo di rompere le bolle che si fprmano durante il riscaldamento della miscela, evitando cosi schizzi nel pallone che distribuirebbe la sostanza ovunque); scaldiamo la miscela, e , dopo qualche minuto, iniziamo vedere la sua evaporazione.
A seconda della temperatura in cui ci troviamo vedremo, passando per il raccordo a tre vie e per il refrigerante, distillare le varie sostanzeda noi cercate: a 64°C l'alcol metilico, a 78°C l'alcol etilico . e così via fino all'acqua.
Prenderemo nota della temperatura ogni 2.5 ml di distillato.
RACCOLTA DATI
PROPRIETA' DI ALCUNI TRA GLI ALCOLI PIU' IMPORTANTI
|
DENOMINAZIONE |
|
FORMULA |
PUNTO DI EBOLIZIONE (°C) |
PUNTO DI FUSIONE (°C) |
DENSITA' (g/cm3) (a 20°C) |
|
corrente |
ufficiale |
|
|
|
|
|
METILICO |
metanolo |
CH3OH |
|
|
|
|
ETILICO |
etanolo |
CH3CH2OH |
-l14 |
|
|
|
n-PROPILICO |
propan-l-olo |
CH3CH2CH2OH |
-l26 |
|
|
|
iso-PROPLICO |
propan-2-olo |
CH3CH(OH)CH3 |
|
|
|
BUTILICO |
butan-l-olo |
CH3CH2CH2CH2OH |
|
|
|
|
iso-BUTILICO |
2-metilpropan-l-olo |
(CH3)2CHCH2OH |
-l80 |
|
|
|
TEMPERATURA (°C) |
MILLILITRI |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Con questo esperimento si intuisce che l'alcoll raggiunge l'ebolizione sui 90°C ad una temperatura minore dell'acqua, e, inoltre siamo riusci a separare gli alcoli dalla parte colorata.
ALCOLI:
composti organici caratterizzati dal gruppo ossidrile -OH, di formula generale R-OH (dove R è un radicale alchilico).
Caratteristiche chimiche
La presenza del gruppo ossidrile fa si che le molecole degli alcoli possano legarsi fra loro con legami a idrogeno; gli alcoli più semplici sono perciò liquidi. Inoltre, l'affinità del gruppo -OH con lìacqua fa si che i primi termini della serie (a.metilico,etilico e propilico) siamno totalmente solubili in esso. Gli alcoli sono facilmente suscettibili all'ossidazione, con formazione di aldeidi o chetoni o acidi carbossilici e danno luogo a varie reazioni, come la perdita di molecole d'acqua (disidratazione) con formazione di alcheni, o la sostituzione dell'idrogeno del gruppo -OH, con radicali alchilici o alogeni, dando eteri o alogenuri alchilici. Industrialmente, gli alcoli vengono ottenuti con processi di fermentazione (per esempio dalla barbabietola), o per via chimica ( per esempio per somma di acqua agli alcheni).
Impieghi
vanno dalla fabbricazione di importanti derivati (come gli esteri e gli acidi carbossilici), in vista della sintesi di molecole piu complesse, all'utilizo diretto come solventi,lubrificanti, anticongelanti,antischiuma, ecc. Non bisogna dimenticare, poi, l'arte, conosciuta fin dall'antichità, di far fermentare alimenti come l'uva, l'orzo, la canna da zucchero per ottenere bevande alcoliche, richhe di alcol etilico. Questo, oltre ad essere usato come antisettico, è stato recentemente impiegato come carburante alternativo alla benzina.
DETERMINAZIONE DELL'ACIDITA' DEL VINO
SCOPO: determinare l'acidità del vino calcolando la quantità in grammi di acido tartarico presente nel campione, in quanto l'acidità fissa dipende dalla quantità di acido tartarico
OH OH
½ ½
Acido tartarico COOH ¾ C ¾ C ¾ COOH
(2,3 - diidrossibutadioico) ½ ½
H H
REAGENTI:
1°Fase:vino bianco (torre di ghiaia);
2°Fase: vino rosso (casereccio).
1° FASE:
2 burette (p:50ml ; s:0.1ml)
agitatore magnetico;
piastra riscaldante;
cartina indicatrice;
beker (50-l00ml)
2°FASE:
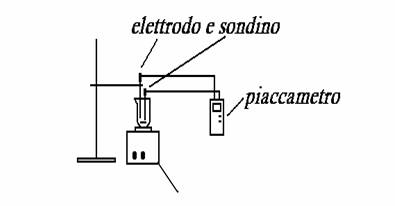
piaccametro;
elettrodo;
sondino;
beker;
agitatore magnetico (ancoretta);
pipetta a bolla(p:25ml ; s:0.1ml)
buretta;
asta di sostegno;
pinze.
pHMETRO
1°Fase:
prelevare 25ml di vino con l'utilizzo di una buretta e trasferirlo in un beker, mescolare per circa 5 minuti, aggiungere circa 25 ml di acqua demineralizzata e tre gocce di fenolftaleina.
Titolare con NaOH 0.25M fino ad un pH compresotra 8 e 9, visualizzando con la cartina indicatrice, ripetere questo procedimento per 3 volte; ed in fine calcolare i grammi di acido tartarico per litro.
2°Fase:
procedere come nella prima fase con l'utilizzo della pipetta al posto della buretta, arrivare ad un pH di 8.2 e utilizzare il piaccametro:
RACCOLTA ED ELABORAZIONE DATI
1°Fase
|
TITOLAZIONE |
V NaOH (L) |
V Vino (L) |
M.E. (g/eq) |
|
g/25ml |
g/1L |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Calcoli
g acido tartarico = N x V x g/eq
g acido x 25 ml = 0,0082 L x 0,25 N x 75,0 g/eq = 0,154 g
g acido x 1 L = 0,154 g x 40 = 6,15 g
2°Fase
|
TITOLAZIONE |
V NaOH (L) |
V Vino (L) |
M.E. (g/eq) |
N NaOH (eq/L) |
g/25ml |
g/1L |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Calcoli
Media vol. NaOH = (0,0080 + 0,0079) / 2 = 0,00795 L
g acido x 25 ml = 0,250 N x 0,00795 L x 75,0 g/eq = 0,149 g
g acido x 1 L = 0,149 g x 40 = 5,96 g
DISTILLAZIONE FRAZIONATA DEL DISTILLATO
SCOPO : Separare i componenti del distillato ottenuto dalla distillazione del vino
REAGENTI: distillato
MATERIALE
distillatore (con colonna di frazionamento)
pinze di sostegno per la colonna
asta di sostegno (o asta a ragno)
serie di provette
ebollitori.
PROCEDIMENTO
Segnare sulle provette i ml da distillare(5 provette con 0,5 ml; 2 con 1 ml; 2 con 2 ml; 2 con 3 ml).
Il procedimento è analogo all'esperienze precedente con la differenze che ogni qual volta il distillato raggiunge il volume segnato sulla provetta, si deve annotare la temperatura raggiunta e cambiare provetta.
RACCOLTA ED ELABORAZIONE DATI
|
TEMPERATURA (°C) |
VOLUME DISTILLATO (ml) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Grazie all'utilizzo della colonna di frazionamento, siamo riusciti, eliminando la testa(cioè la parte iniziale distillata) e la coda (la parte finale distillata), ad ottenere 6ml di grappa.
I
L VINO
Bevanda alcolica ottenuta dalla fermentazione del mosto d'uva. Da un punto di vista chimico, è una miscela di acqua (85-90%), alcol etilico (5-l5%) e altre sostanze (acidi tartarico e lattico, glicerina, tannino ecc.) che gli conferiscono le caratteristiche organolettiche. Il vino si ottiene dall'uva mediante il processo di vinificazione. Questo inizia con la pigiatura, che trasforma l'uva in mosto; tale mosto passa poi nei tini dove ha inizio la fermentazione, durante la quale, per mezzo dell'enzima prodotto dal micete Saccharomyces ellipsoideus, gli zuccheri vengono scomposti in alcol e anidride carbonica. Per separare il vino dalle vinacce, si procede poi alla svinatura che si esegue pompando il vino dai tini nelle botti. Cessata la fermentazione lenta del vino nelle botti, si iniziano i travasi e quindi si procede all'imbottigliamento, che nei vini di minor pregio può essere preceduto o seguito da un processo di pastorizzazione.
DETERMINAZIONE DEL GRADO ALCOLICO
Il grado alcolico viene definito come il titolo alcolometro - volumico, cioè la percentuale di alcool misurata in volume. I metodi per calcolare il grado alcolico sono i seguenti:
metodo ebulliometrico;
metodo per distillazione;
metodo con alcolometro;
L'alcolometro è provvisto di una scala espressa in ° alcolici (da 0 a 100); la scala dà un ° apparente che deve essere corretto in relazione alla temperatura in °C di esperienza poiché l'alcolometro è tarato a 15°C. Apposite tabelle permettono di risalire dal ° alcolico al ° reale.
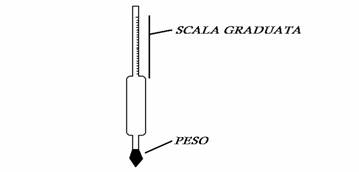
ESPERIENZA:
L'alcolometro viene messo nel campione da analizzare e dopo alcuni secondi si legge il risultato sulla scala; esso non deve toccare le pareti del contenitore in cui è posto il campione.
VINI UTILIZZATI |
° APPARENTE |
TEMPERATURA °C |
° REALE |
|
Cannonau |
|
|
|
|
Bianco |
|
|
|
|
Barbera |
|
|
|
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta