| chimica |
|
|||||
|
Coloranti rossi di origine animale
Il rosso Carminio o di Cocciniglia & la Porpora
![]()
Introduzione
Gli esseri umani hanno sempre avuto un rapporto speciale con il rosso. Diversi antropologi hanno dimostrato che, nella maggior parte delle culture, i primi nomi riferiti ai colori distinguevano tra chiaro e scuro; poi quando una lingua si evolveva fino a comprendere tre nomi di colori, comunemente il terzo termine si riferiva al rosso.
Durante il Medioevo l'importanza del colore rosso non si limitava alla sua affinità con la natura ma era apprezzato perché era relativamente raro. I tintori medievali, estremamente abili e preparati, riuscivano a produrre molti colori ma il rosso era molto difficile da ottenere, almeno in forma duratura. Non era raro che presso una tintoria medioevale tingere una stoffa di rosso costasse dieci volte di più che tingerla d'azzurro.
È interessante notare che nel secolo XIX l'accesso a tinture più commerciali e a basso costo portò un cambiamento nel valore culturale attribuito al rosso. Stabilità, diffusione, e la disponibilità dei nuovi prodotti, ottenuti mediante opportuni procedimenti di sintesi, determinarono un certo declino dei rossi e in genere di tutti i colori di origine naturale. A ciò si aggiunse un certo disprezzo da parte delle classi d'élite nei confronti di stoffe e paramenti scarlatti, poiché questo colore era ormai molto popolare tra immigranti, appartenenti alla classe operaia e persone di colore. I nobili europei inorriditi quindi all'idea di confondersi con il volgo, voltarono le spalle al rosso, sostituendolo con il nero, il blu, il grigio e i colori pastello.
Il declino del rosso fu dovuto anche al suo antico legame con violenza e passione. Per secoli quest'associazione era stata contrastata dalle principali caratteristiche del colore: la sua rarità, la sua bellezza e il suo legame con il potere e con lo status. Ma quando il rosso non fu più così raro, queste vecchie idee riemersero, e nella mente dei ceti più abbienti, esso fu associato alla volgarità, alla promiscuità e ad un basso ceto sociale.
Coloranti e Pigmenti
I materiali colorati per secoli utilizzati nella tintura delle stoffe sono definiti Coloranti e sono ben differenti dai Pigmenti. I Coloranti, infatti, sono sostanze trasparenti, solubili, capaci di impartire il proprio colore ad altre non colorate, per inclusione, assorbimento o attraverso la formazione di legami chimici stabili con esse.
I pigmenti invece sono costituiti da polveri fini, colorate, insolubili nel veicolo disperdente con il quale formano un impasto più o meno denso che anche quando è steso in uno strato sottile manifesta proprietà coprenti.
Oltre ad aver trovato un importante impiego nella tintura dei tessili, operazione nella quale, tipicamente, la sostanza colorata trasferisce questa sua proprietà ad un altro materiale incolore detto fibra, i coloranti trovarono un valido utilizzo per la preparazione delle lacche in pittura, e più recentemente nel campo alimentare e nella cosmesi.
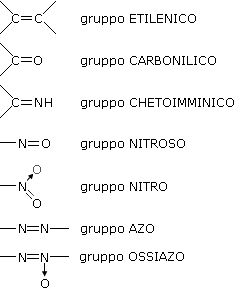
La capacità di un colorante di assolvere la sua azione è dovuta alla presenza nel composto di due gruppi funzionali, uno responsabile del colore e l'altro responsabile della fissazione sul supporto. Rispettivamente sono detti cromoforo, quello conferente il colore e auxocromo quello legante la molecola del colorante al substrato da tingere, e responsabile di una buona diluizione del colorante in un dato solvente.
Il termine colore descrive una sensazione fisiologica, soggettiva, dell'occhio umano che è sensibile alle sole radiazioni elettromagnetiche dello spettro comprese nell'intervallo tra 400 e 700 nm circa. Tale sensazione è il risultato della combinazione di differenti fattori: tipo d'illuminazione, sensibilità dell'occhio nei confronti delle radiazioni e modificazioni provocate dalla materia dell'oggetto sull'insieme di radiazioni visibili incidenti su di esso. Perché una sostanza appaia colorata occorre quindi che le molecole di cui è composta assorbano radiazioni elettromagnetiche nel campo del visibile. Le radiazioni dello spettro visibile hanno, infatti, potenzialmente un'energia sufficiente ad eccitare alcuni elettroni di legame a bassa energia o elettroni mobili presenti nelle sostanze che appaiono colorate. Quando queste sono investite da una luce bianca, possono risultare selettivamente assorbite alcune radiazioni che possiedono l'energia necessaria all'eccitazione degli elettroni mobili. Alla luce bianca incidente vengono in questo modo sottratte le radiazioni assorbite dal corpo col risultato che la porzione del raggio che viene riflessa non stimola più la sensazione di saturazione del bianco ma quella d'altri colori. I gruppi cromofori presenti nei coloranti hanno appunto la capacità aumentare la lamda d'assorbimento del composto, portando cosi il colore che noi osserviamo, complementare a quello d'assorbimento, nel campo del visibile. I gruppi cromofori più comuni all'interno delle molecole dei coloranti sono:
L'auxocromo è il gruppo che legherà la molecola al
substrato da tingere e in genere è anche il responsabile della solubilità. I
principali auxocromi sono il gruppo ossidrilico -OH e i suoi derivati come -OR,
il gruppo amminico -NH![]() e
suoi derivati come -NHR, -NR
e
suoi derivati come -NHR, -NR![]() ,
-NHC
,
-NHC![]() H
H![]() ,
-NHOH, -NH-NH-, il gruppo solfonico -SO
,
-NHOH, -NH-NH-, il gruppo solfonico -SO![]() H e
il gruppo carbossilico -COOH.
H e
il gruppo carbossilico -COOH.
Gli auxocromi oltre a permettere la fissazione della molecola sono in grado di aumentare il valore della lunghezza d'onda della radiazione assorbita in modo da portare nel campo del visibile una molecola che prima assorbiva nel campo dell'UV, e per questo non appariva colorata, oppure di aumentare l'intensità di colore.
In riferimento alla costituzione chimica i coloranti possono essere ordinati in: azo coloranti, nitroso coloranti, nitro coloranti, coloranti del difenilmetano, coloranti del trifenilmetano, coloranti indigoidi, coloranti atrachinonici, coloranti dello stilbene, coloranti azinici, coloranti ossazinici, coloranti tiazinici, coloranti della mono e triclorotriazina. Secondo la tecnica d'applicazione è possibile classificarli in: coloranti acidi, coloranti basici, coloranti diretti, coloranti sostantivi, coloranti a mordente, coloranti premetallizzati, coloranti reattivi, coloranti allo zolfo, coloranti al tino.
Il rosso Carminio o di Cocciniglia
La scoperta dell'America da parte della Sna aprì le porte verso un nuovo mondo, pieno di ricchezze sconosciute all'Europa del tempo. Una di loro era la cocciniglia, un piccolo insetto che abbondava in un tipo di cactus che cresceva in Messico. In diversi documenti contenuti negli archivi snoli spesso si fa riferimento alla parola "grana" o "grana cochinilla", come una tra le principali merci che la Sna importava dal nuovo Mondo, la più preziosa dopo l'oro e l'argento. La cocciniglia presentava una serie di vantaggi sulle tinture utilizzate a quell'epoca in Europa. Grazie alla sua composizione chimica, essa produceva un rosso più ricco e duraturo ed era più facile da coltivare, per lo meno in Messico. In Europa le radici che producevano la 'robbia', un colorante rosso, erano conosciute sin dall'antichità, ma il colore era soggetto a leggere variazioni di alcalinità e di temperatura. Tinture prodotte da insetti della famiglia delle cocciniglie quali il chermes, il sangue di San Giovanni e il rosso armeno erano molto ricercate ma difficili da ottenere. Non è quindi difficile comprendere come già nel 1570 l'industria tessile europea si era convertita all'uso della cocciniglia, dalla quale era diventata dipendente.
Attualmente sta tornando molto forte la richiesta di coloranti naturali non nocivi alla salute. Ai giorni d'oggi circa l'85% delle scorte mondiali di cocciniglia sono prodotte dal Perù.
Le cocciniglie o Pseudococcidae sono una famiglia di insetti parassiti delle piante. La specie è talmente ampia che risulta più facile, nella nomenclatura d'uso corrente, identificare le varie tipologie di cocciniglia con la pianta ospite. Di varie forme e con una gran varietà di cicli biologici, possono avere colorazioni che vanno dal bruno-rossastro al bianco. Sono però tutte accomunate dall'avere dimensioni racchiuse dai pochi millimetri al mezzo centimetro. Riconoscere le cocciniglie non è difficile, sono infatti molto diverse dagli insetti comunemente visibili, in quanto si ricoprono di una patina cerosa che usano per proteggersi, formando uno scudo protettivo, solitamente bianco, che può essere gommoso oppure rigido a seconda della specie. Tra le varietà di cocciniglia più diffuse ci sono le Iceria Saissetia distinguibili grazie al loro scudo esterno rigido spesso scuro, le Ceroplastes protette da scudo ceroso, le Chloropulvinaria chiamate comunemente cocciniglia fioccosa, e le Pseudococcus e ococcus comunemente chiamate cocciniglia farinosa.
Le cocciniglie attaccano prevalentemente le conifere, le succulente, le piante ornamentali, la vite e gli agrumi; si sviluppano al meglio nelle zone della pianta in cui filtra poca luce, poca umidità e poca ventilazione. La maggior parte delle cocciniglie si annidano su fusti giovani e sulle foglie, nutrendosi di linfa ricca di sostanze zuccherine perforando con un rostro la superficie; alcune specie colonizzano anche le radici causando danni ingenti alle piante.
Il rosso carminio e la lacca di cocciniglia sono ottenuti a partire dai corpi essiccati della femmina del Coccus Cacti che viene coltivato prevalentemente nelle piantagioni di cactus (Nopalea coccinillifera) dell'America Centrale e del Sud America. Sono estratti in soluzioni acquose con variazioni di colore che partono dall'arancione fino a giungere al rosso. Il principio colorante del carminio è la forma alluminio chelata idratata dell'acido carminico, nella quale l'alluminio e l'acido carminico sono presenti con una molarità pari a 1:2. L'acido carminico viene estratto facendo bollire un kg di colorante con 30 g di potassa in un litro d'acqua con allume. Un ettaro di terreno coltivato a cactus produce all'anno circa 300 kg di cocciniglia equivalenti a 2 kg di colorante. In commercio il principio colorante è venduto in associazione con i cationi di ammonio, calcio, potassio o sodio, presenti singolarmente o combinati, spesso anche in eccesso. L'ammonio carminio possiede una solubilità in un ampio intervallo di pH, mentre il calcio carminio presenta una solubilità limitata in soluzioni a pH acido. Inoltre i prodotti sul mercato, contengono "particelle" proteiche derivate dagli insetti, e possono contenere anche anioni carminato liberi o piccoli eccessi di cationi alluminato.
Oltre al grande utilizzo nel campo tessile, e nelle opere pittoriche del passato, l'acido carminio è oggi utilizzato, grazie alla sua grande resistenza a luce e calore, in prodotti alimentari a basso pH come bibite e dolciumi. Recenti studi evidenziano come l'ammonio carminio è generalmente utilizzato nell'industria alimentare come colorante per le bibite alcoliche, mentre il calcio carminio è utilizzato nei cibi, senza significanti effetti tossicologici per l'uomo.
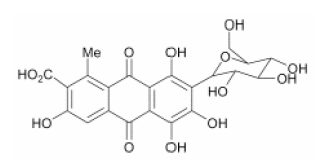

Acido carminico (C22H20O13)
 L'acido
carminio è costituito da un glucoside chiamato cocciniglina, poliossiacido
antrachinonico in cui un ossidrile è legato ad uno zucchero. La Cociniglina non
viene più usata data la scarsa solidità all'acqua, agli acidi e agli alcali. Il
carminio appartiene alla classe di coloranti chiamati antrachinonici. Questa classe di coloranti si identifica grazie
alla presenza di un gruppo cromoforo antrachinonico inserito in un sistema più
o meno complesso. Tecnicamente possono essere coloranti acidi, a mordente, al
tino, a dispersione, pigmenti o lacche. I coloranti a mordente di questa serie
sono in genere poligenetici le cui tonalità variano dal rosso al porpora al blu
in funzione del metallo complessato. Il più noto della serie è il rosso
mordente 11 o alizarina
L'acido
carminio è costituito da un glucoside chiamato cocciniglina, poliossiacido
antrachinonico in cui un ossidrile è legato ad uno zucchero. La Cociniglina non
viene più usata data la scarsa solidità all'acqua, agli acidi e agli alcali. Il
carminio appartiene alla classe di coloranti chiamati antrachinonici. Questa classe di coloranti si identifica grazie
alla presenza di un gruppo cromoforo antrachinonico inserito in un sistema più
o meno complesso. Tecnicamente possono essere coloranti acidi, a mordente, al
tino, a dispersione, pigmenti o lacche. I coloranti a mordente di questa serie
sono in genere poligenetici le cui tonalità variano dal rosso al porpora al blu
in funzione del metallo complessato. Il più noto della serie è il rosso
mordente 11 o alizarina
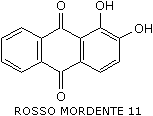
L'alizarina, un tempo estratta dalla Robbia, è stata verso il XIX secolo sostituita dall'Alizirin Crimson o Alizarina artificiale. Si tratta di un tipico colorante a mordente poligenetico, il quale forma con Ca, Ba e Sr delle lacche rosso porpora, con Al rosso-rosa, con Cr e Cu lacche bruno violetto, con Fe trivalente e Hg lacche nero-violetta. La più importante lacca dell'alizarina è quella con l'Al ottenuta in presenza di olio di ricino solfonato e prende il nome di rosso turco o rosso di Adrianopoli. Come per il rosso carminio si tratta di una lacca premetallizzata con alluminio in molarità 1:2.
Sono detti coloranti a mordente i coloranti in grado di complessarsi con un metallo, per questo il processo di tintura con questi prodotti viene detto mordenzatura. La reazione colorante-metallo viene detta metallizzazione e può avvenire nel bagno di tintura o essere già stata fatta precedentemente; in questo caso i coloranti prendono il nome di premetallizzati come le lacche dell'Alizarina e la lacca di Cocciniglia. Una classificazione di questi coloranti viene fatta a seconda del rapporto tra atomi di metallo e molecole di colorante presenti nel complesso. Si distinguono così:
v coloranti 1:1, cioè una molecola di colorante ogni atomo di metallo
v coloranti 1:2, cioè due molecole di colorante ogni atomo di metallo
v coloranti 2:3, si tratta di una combinazione di un complesso 1:2 e uno 1:1
|
|
|
|
|
|
|
|
esempio di complesso 1:1 |
|
esempio di complesso 1:2 |
|
Il premetallizzato del tipo 1:2 è di dimensioni notevoli rispetto a quello 1:1 e per questo presenta solo un effetto di tintura superficiale. Nei coloranti della serie 1:1 il metallo è in grado di instaurare dei legami secondari con la fibra, aumentando in questo modo la coesione è donando al colorante caratteristiche tintoriali maggiori. I tessuti tinti con coloranti a mordente delle serie 1:1 sono infatti più resistenti allo strofinio e ai lavaggi. Per quanto riguarda i complessi 1:2 il metallo è completamente circondato dal colorante e non è quindi capace di instaurare legami secondari con la fibra; l'azione fissativa avviene esclusivamente ad opera dei gruppi auxocromo presenti nella molecola del colorante.
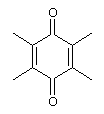
Altri coloranti a mordente della serie dell'alizarina sono l'arancio mordente 14 o arancio alizarina e il bruno mordente 42
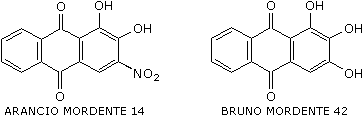
Dalle formule dei due coloranti e dai loro toni possiamo notare come varia il colore col cambiamento dei sostituenti. Il gruppo nitro è un elettron-attrattore quindi è necessaria più energia per far avvenire la transizione, l'assorbimento si sposterà verso il blu e quindi il complementare verso toni più chiari.
I coloranti acidi di questa serie si ottengono per solfonazione dei rispettivi coloranti a mordente; quelli al tino invece derivano dalla riduzione del gruppo antrachinonico a fenolico dove successivamente verrà ripristinato il cromoforo chinonico.
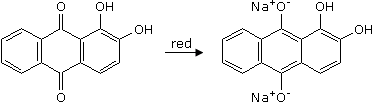
Anche in questo caso i coloranti al tino sono resistenti al lavaggio ma non molto agli ossidanti.
La lacca di Kermes
La lacca di Kermes è nota anche come Chermes, Kermes Lake, Grana o Crimson Lake. Il kermes è la femmina di un insetto della famiglia delle cocciniglie, conosciuto con il nome di Coccus ilicis. Come per le cocciniglie da cui si estrae il rosso di carminio, le Coccus ilicis per nutrirsi sfruttano la linfa zuccherina delle piante sui cui vivono. In Europa è possibile incontrarle soprattutto sulla Quercus coccifera, un piccolo leccio tipico della Francia del sud, della Sna, e della Sicilia. Il colorante che se ne ricava fu molto usato in epoca Medievale, quando la sua diffusione porto al progressivo declino dell'uso della porpora. Nonostante l'elevato costo, la lacca di Kermes, fu per diversi secoli il colorante rosso più usato e apprezzato in assoluto, basti pensare che a partire dal'400 ad opera di Papa Paolo II le vesti dei cardinali saranno tinte con il rosso di kermes, anziché con la porpora cardinalizia.
Differentemente dalla lacca di Cocciniglia, prodotta attraverso la lavorazione del corpo delle Coccus Cacti, la lacca di Kermes viene estratta dalle uova degli insetti. Dopo la fecondazione le uova ricche del principio colorante rimangono aderenti all'animale, il processo per la produzione della lacca prevede che prima che le femmine muoiano vengano raccolte le uova. Queste saranno spruzzate con una soluzione acida come l'aceto o succhi di vegetali acerbi ed essiccate acquisendo l'aspetto di piccole sfere leggere e friabili, di colore rosso scuro, spesso coperte di polvere biancastra. Bagnando i granelli in acqua si estrae l'acido chermesico, principio colorante rosso, variante nel tono dall'arancio al purpureo, a seconda che il liquido venga acidificato o alcalinizzato.
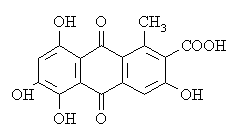
Acido chermesico
L'acido chermesico appartiene come l'acido carminico alla classe di coloranti antrachinonici. In passato la tintura delle stoffe di fibra animale era realizzata per mezzo di mordenti che uniti all'acido davano diverse sfumature di rosso: l'allume dava un color cremisi, lo stagno dava un colore scarlatto, e il ferro dava un colore porpora. Inoltre la buona solubilità in acqua consente di ottenere una tonalità gialla in presenza di acidi, e una tonalità rossa più o meno bruna in presenza di alcali. Attualmente l'acido chermesico è prodotto sinteticamente attraverso l'idrolisi dell'antrachinone.
La Porpora
La porpora era in età imperiale il colore per eccellenza. Esso veniva estratto dai molluschi detti murici o comunemente porpora. Per riuscire a tingere anche solo una veste o una tunica occorrevano migliaia d'esemplari. Da ogni mollusco era infatti possibile estrarre una sola goccia di colorante; da ciò e dalla scarsa disponibilità di materia prima, derivava in parte la sua preziosità.
Il prezioso colorante purpureo era ottenuto trattando con acqua e urina il liquido estratto da dei molluschi conchiferi dei generi Murex e Nucella. I più noti e usati erano il Murex trunculus, il Murex brandaris e la Purpura haemastoma. Anche da Nocella lapillus e Buccinum echinophorum si poteva estrarre la nota sostanza. Nell'Oceano Pacifico è diffusa la Purpura papula pansa Gould, sulla costa atlantica la Purpura papula Linnè, leggermente diversa dalla precedente per forma e colore.
Gli antichi naturalisti ignoravano le proprietà fotografiche, che si riscontrano nella materia porporigena che vi si può estrarre, per cui la tinta violetta si genera essenzialmente per l'azione chimica della luce. La porpora ebbe molto successo presso gli antichi, non solo per la sua bellezza, ma anche per la sua resistenza.
La tinta della porpora, più o meno violacea, poteva variare in base alla specie della conchiglia e - secondo Vitruvio - a seconda del luogo e del clima: la porpora del Ponto e della Galatea, regioni nordiche, era scura, mentre quella delle regioni nord-occidentali era livida. Tra l'oriente e l'occidente equinoziale si trovava una porpora violacea; quella dei paesi meridionali era invece rossa. Il colorante dato dal M. brandaris era brillante e tendente al rosso, invece quello del M. trunculus virava al blu. La sapiente sovrapposizione dei vari coloranti eseguita dai tintori, permetteva di ottenere un gran numero di gradazioni differenti.
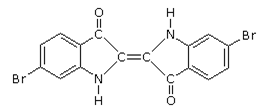 Il principio colorante della porpora è il dibromoindaco. La
composizione chimica di questo colorante e molto simile a quella di un
colorante blu di origine vegetale, l'indaco, dal quale differisce per due soli
atomi. Al posto dei due atomi di bromo della porpora, l'indaco possiede infatti
due atomi di idrogeno. Secondo alcuni scritti sembra che le lumache del genere Trunculariopsis
trunculus secernano sia il colorante indaco che il dibromoindaco, in
funzione del sesso dell'animale. Gli ebrei impiegando i coloranti estratti da
queste lumache, fabbricavano un colore detto tekhelet, impiegato per tingere le
frange dei loro indumenti.
Il principio colorante della porpora è il dibromoindaco. La
composizione chimica di questo colorante e molto simile a quella di un
colorante blu di origine vegetale, l'indaco, dal quale differisce per due soli
atomi. Al posto dei due atomi di bromo della porpora, l'indaco possiede infatti
due atomi di idrogeno. Secondo alcuni scritti sembra che le lumache del genere Trunculariopsis
trunculus secernano sia il colorante indaco che il dibromoindaco, in
funzione del sesso dell'animale. Gli ebrei impiegando i coloranti estratti da
queste lumache, fabbricavano un colore detto tekhelet, impiegato per tingere le
frange dei loro indumenti.
Probabilmente, a causa della scarsità e del costo della materia prima, i tintori fecero uso anche di pseudo-porpore, estratte da alcuni sottogeneri di Aplysia Linnaeus, le quali presentano una composizione chimica completamente differente da quella della porpora propriamente detta, appartenendo al genere delle porfirine, con struttura tetrapirrolica non ciclica. L'aplysioporporina è infatti una miscela di due bilicromoproteine: l'aplysioviolina (viola) e l'aplysiordina (rossa), il cui colorante principale è la bilirubina una sostanza di colore giallo-rosso che rappresenta il prodotto di degradazione dell'emoglobina, pigmento scarlatto presente nei globuli rossi del sangue.
L'estrazione del colorante
I murici dovevano essere catturati vivi nel periodo compreso fra l'autunno e la primavera, lontano dal periodo della filiazione. Per ottenere il liquido porpurigeno bisognava sacrificarli tagliandoli, e raccogliendo il prezioso succo fuoriuscito dalla vena bianca in un mortaio. Gli esemplari più grandi venivano estratti dalla conchiglia, mentre i più piccoli venivano frantumati vivi con la mola. Aristotele, in "Historia animalium" racconta che il "fiore" dell'animale è situato tra il fegato e il collo, e l'attaccamento reciproco di questi è molto stretto. Il mollusco battuto e tagliato emette allora delle gocce di color porpora che si raccolgono per generare il colore. Alla poltiglia così raccolta si aggiungeva del sale marino o acqua di mare, e si lasciava macerare il composto per tre giorni al sole in maniera tale che il liquido si separasse dal resto. Quindi bisognava aggiungere un grande quantitativo d'acqua e cuocere a calore moderato, schiumando i resti degli animali che venivano via via a galla. Il composto doveva bollire per dieci giorni in vasi di piombo fintanto che risultasse ridotto almeno della metà e non fosse diventato abbastanza fluido. A questo punto si potevano immergere le stoffe di lino o di lana che successivamente venivano esposte all'aria per provocare l'ossidazione allo scopo di raggiungere la tinta rossastra.
La sostanza appena estratta è densa e dall'odore nauseante, presenta un colore giallo pallido e grazie all'azione della luce, muta in verde, blu e poi rosso, per giungere infine ad un tono purpureo. In tutte le specie purpurigene il pessimo odore che si avverte durante la lavorazione è causato dalla presenza nei gruppi protocromogeni di un radicale solforico o un gruppo mercaptamogenico.
Se il composto è tenuto al buio, si possono ottenere delle porpore gialle o verdi.
Il colorante porpora veniva usato anche per realizzare una lacca, il purpurissum di Plinio.
Oggi .
Vengono tagliati i murici e con le forbici si staccano le borse che contengono l'umore porporigeno. Con esse e con il liquido che contengono si fa una poltiglia, che viene fatta asciugare all'aria finché non diventa violetta e disseccata, per poter poi, essere polverizzata e conservata in appositi contenitori. Successivamente, si lava ripetutamente con acido acetico cristallizzabile, il quale discioglie la porpora. Ottenuto ciò, si diluisce con molta acqua, sino a che la soluzione non diventi lattiginosa e quasi scolorita. Infine viene agitata con il cloroformio, che separa la porpora dal liquido acquoso. Dopo un lungo riposo il cloroformio si raccoglie sul fondo del vaso, di colore azzurro o violetto a seconda della quantità di porpora che contiene. Quindi si divide il cloroformio dalla soluzione acquosa, si filtra ed infine si evapora ad una temperatura di 25°. Ciò che rimane dall'evaporazione è un composto solido, cristallino, di colore azzurro con riflessi metallici.
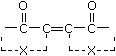 Il dibromoindaco, principio colorante
della porpora appartiene alla categoria dei coloranti indigoidi, il cui nome è dovuto all'indaco, colorante naturale
caratterizzato dal cromoforo a lato, dove X è un gruppo aromatico più o meno
complesso. Rispetto al doppio legame può essere individuato un piano di
simmetria e quindi i coloranti si possono distinguere in simmetrici ed
asimmetrici, a seconda che X sia uguale da entrambe le parti o diverso.
Il dibromoindaco, principio colorante
della porpora appartiene alla categoria dei coloranti indigoidi, il cui nome è dovuto all'indaco, colorante naturale
caratterizzato dal cromoforo a lato, dove X è un gruppo aromatico più o meno
complesso. Rispetto al doppio legame può essere individuato un piano di
simmetria e quindi i coloranti si possono distinguere in simmetrici ed
asimmetrici, a seconda che X sia uguale da entrambe le parti o diverso.
Dato che è presente un doppio legame possono
esistere due forme isomere (cisoide e transoide).
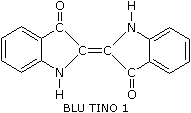
Il più semplice rappresentante di questa classe è l'indaco il cui derivato
sintetico si chiama blu tino 1.
L'indaco può essere estratto da vegetali sotto forma di glucoside, detto anche indicano, si tratta di un estere col glucosio che viene idrolizzato con acqua ottenendo in questo modo glucosio e indossile, il quale per ossidazione in aria darà l'indaco.
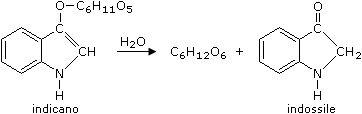
L'indaco più pregiato era estratto da alcune piante del genere Indigofera, fra cui l'Indigofera tinctoria, l'I. leptostachya e l'I.anil, piante appartenenti alla famiglia delle papillonacee. L'Isatis tinctoria è un'erba spontanea, piuttosto robusta, la cui altezza può variare dai 40 ai 120 centimetri. I fiori sono gialli e le foglie sono di due tipi: quelle radicali sono piccole e ovate, mentre quelle del fusto sono bislunghe e abbracciano il fusto stesso. Secondo la ricetta maggiormente divulgata, inerente all'Indigofera, i fusti e particolarmente le foglie delle piante dovevano essere raccolte nel periodo della fioritura e immerse in acqua, lasciandole macerare per una notte affinché l'indacano glucoside dell'indigotina si scindesse in glucosio e indossile incolore. Trascorso tale tempo, la soluzione veniva agitata al fine di favorirne i processi di ossidazione, con la conseguente formazione di fiocchi di indigotina (blu) che andavano a depositarsi sul fondo del contenitore insieme ad altre sostanze coloranti: l'indirubina o rosso d'indaco, il bruno d'indaco (sostanza bruna solubile in acqua), il canferolo o giallo d'indaco (un derivato flavonico), sostanze azotate (glutine d'indaco) e ceneri. Il processo di fermentazione avveniva grazie all'azione di enzimi presenti nella pianta e non, come si potrebbe pensare, per tramite di batteri; la loro azione risultava altresì favorita dall'impiego di acqua a temperatura superiore ai 50°C. Il contenuto di indigotina poteva variare da un minimo del 20% a un massimo del 50/60%; quello dell'indirubina si aggirava sul 2/4%.
Oggi l'indaco si ottiene per sintesi, si tratta di una polvere cristallina blu con riflessi ramati che non è solubile in acqua, in acidi o in alcali ma solo in solventi ad alto punto di ebollizione; per queste sue caratteristiche verrebbe classificato più esattamente tra i pigmenti piuttosto che tra i coloranti. Viene utilizzato invece come colorante al tino, si procede infatti ad una ossidazione con soda e solfuro di sodio (o solfito o bisolfito) ottenendo l'indaco ridotto o indaco bianco. L'indaco ridotto è solubile in acqua in ambiente alcalino ed è trasferibile quindi su fibra tramite un bagno.
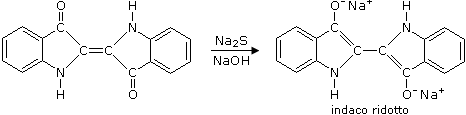
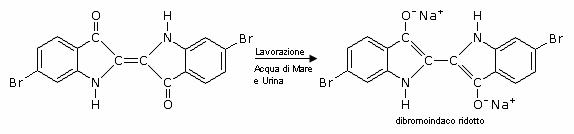
La fibra viene impregnata di indaco ridotto, se ne lava l'eccesso, e si espone il substrato impregnato all'aria provocando l'ossidazione a indaco; si tratta in pratica di una precipitazione microcristallina su fibra. Lo stesso procedimento avveniva nella tintura dei tessuti con porpora dove il dibromoindaco dopo essere stato ridotto durante la lavorazione in acqua salata e urina veniva fatto precipitare sul tessuto.
Lacca da Porpora: il "purpurissum
La porpora ha avuto anche un utilizzo in pittura, e come avviene per tutti i coloranti per questo impiegato veniva tramutata in lacca. A tal fine, come ci ha tramandato Plinio, bisognava immettere nelle caldaie in cui veniva preparata la porpora della creta argentaria in modo che questa ultima assorbisse il colorante. La lacca migliore era la prima, la quale presentava una maggiore concentrazione di colorante che andava diminuendo mano a mano che si aggiungeva creta nella caldaia. Il colore di questa lacca variava da un violetto intenso ad un rosa-violaceo pallido, comprendendo un'ampia gamma di tonalità. Le differenze di tono erano date innanzitutto dalla quantità di materia colorante fissata sulla creta e dalla concentrazione della soluzione con cui la lacca veniva prodotta. In secondo luogo era possibile ottenere lacche più chiare aggiungendo creta bianca calcarea al composto o per rinforzare il tono aggiungendo coloranti d'origine vegetale.
BIBLIOGRAFIA
v P. BALL, Colore - Una biografia, Milano 2004
v AAVV, La fabbrica dei colori, Roma 1995
v M. MATTEINI, A. MOLES, La Chimica nel Restauro, Firenze 2004
v S. BENZI, Lezioni di Chimica Organica (vol. II), Padova 1968
SITI INTERNET CONSULTATI
https://it.wikipedia.org/wiki/Pseudococcidae
https://www.istitutoconciario.com
https://chemfinder.cambridgesoft.com/reference/chemindex.asp
https://www.threemonkeysonline.com/it/article-cocciniglia-rosso.htm
https://www.inchem.org/documents/jecfa/jecmono/v16je09.htm
https://www.auditorium.info/articolo.asp?id=193
https://www.romanhideout.com/legiov/fabrica/porpora_it.asp
https://www.ipsema.it/nautes/nautes33_pdf/26_Arti_e_mare_fondali_4.pdf
|
Privacy
|
© ePerTutti.com : tutti i diritti riservati
:::::
Condizioni Generali - Invia - Contatta